26/03/2023 (2023-03-25)
[Source : truth613.substack.com]
[Traduction Jean Bitterlin]
J’ai été choquée lorsque j’ai découvert ce qui se passait.
Mise à jour le 1er mars à 15h00 avec de nouvelles preuves de l’inefficacité du vaccin contre le papillomavirus dans son objectif déclaré de prévention du cancer du col de l’utérus – voir la fin de l’article.
Après avoir entendu de terribles histoires sur de multiples tragédies en cours résultant directement du vaccin Gardasil dans la ville de Lakewood, dans le New Jersey, où j’ai de nombreux amis, j’ai le sentiment que je dois sensibiliser tout particulièrement aux graves dangers de ce vaccin.
Des adolescents de la communauté de Lakewood, qu’un de mes amis connaît personnellement, sont actuellement couchés dans leur lit, paralysés et complètement handicapés, à cause de ce vaccin anti-HPV empoisonné qui leur a été administré par leur médecin.
D’autres jeunes femmes sont ménopausées et n’ont même plus de follicules à cause du Gardasil. (Voir le procès ci-dessous.)
Que Dieu ait pitié ! Pourquoi ?
Dans quel but a-t-on donné du poison à ces enfants ?
L’objectif déclaré du Gardasil est de prévenir une MST (Maladie Sexuellement Transmissible) qui pourrait éventuellement entraîner un cancer du col de l’utérus lorsque les enfants seront beaucoup plus âgés.
Mais il n’existe aucune preuve que le vaccin soit réellement efficace pour prévenir le cancer. Il s’agit d’une imposture qui ne fait que provoquer la mort et la misère.
Un procès est en cours contre le fabricant du vaccin, Merck. Le cabinet d’avocats est Miller et Zois. Il déclare qu’il examine les actions en justice relatives au vaccin Gardasil dans les 50 États.
(Tout cela pour un vaccin dont le CDC mensonger prétend qu’il y a eu si peu de rapports d’effets indésirables vérifiables qu’il n’a pas pu établir de corrélation !).
Le procès Gardasil accuse Merck d’avoir dissimulé frauduleusement des preuves concernant les risques pour la santé du Gardasil tout en le présentant faussement comme un vaccin pouvant prévenir le cancer du col de l’utérus.
[Voir aussi :
►Gardasil Episode 7 : Entre mensonges et corruptions
►Le Gardasil ne diminue pas la fréquence des cancers du col de l’utérus, ni de l’anus
►Gardasil, un vaccin de moins en moins polémique et de moins en moins dangereux au fil du temps ?
►Gardasil épisode 3 : Dévastateur et pourtant 17 ans sans procès, pourquoi ?
►Les erreurs et/ou mensonges du Parisien sur le Gardasil l’exposeront-ils à des poursuites judiciaires ?
►Gardasil : 10 mensonges dans un seul article de l’AFP Factuel
►Premier procès pour décès injustifié lié au Gardasil, alléguant que le vaccin contre le VPH a causé la mort d’un adolescent de 13 ans
►Ne vaccinons pas non plus les garçons par le Gardasil
►Avalanche de « Fake news » pour promouvoir le Gardasil chez les garçons
►Merck pousse le vaccin mortel Gardasil sur les enfants de 9 ans pour augmenter les ventes — Vaccin connu pour causer l’infertilité]
Le procès Gardasil
[Source : millerandzois.com]
Nos avocats examinent les actions en justice relatives au vaccin Gardasil dans les 50 États pour les victimes qui ont souffert des effets secondaires du vaccin Gardasil contre le papillomavirus. Des décès et des blessures ont été liés à ce vaccin. Notre cabinet d’avocats étudie différents types de procès concernant le vaccin Gardasil, en se concentrant sur les plaintes relatives à l’insuffisance ovarienne prématurée et à la ménopause prématurée.
Cette page a pour but de vous aider à mieux comprendre si vous souhaitez intenter une action en justice concernant Gardasil et si vous pouvez prétendre à un règlement ou à un paiement par un jury. Il s’agit d’un nouveau litige et nos avocats mettent régulièrement cette page à jour (dernière mise à jour : 9 février 2023) pour vous apporter les dernières nouvelles et mises à jour concernant le procès Gardasil HPV.
Mises à jour sur le recours collectif contre le vaccin HPV Gardasil
Mise à jour mars 2023
- 1er mars 2023 : Outre les affaires Gardasil en cours dans le MDL devant les tribunaux fédéraux, un grand nombre de procès concernant le vaccin Gardasil sont en cours devant les tribunaux de l’État de Californie. Bon nombre de ces procès ont été intentés en premier et un certain nombre d’entre eux devaient être jugés à partir du mois de septembre de cette année. Malheureusement, toutes ces dates de procès ont été reportées à septembre 2024. Ce report a été effectué afin de coordonner l’avancement du procès Gardasil en Californie avec le calendrier du MDL NdT : Le Multidistrict litigation (MDL) – litigation pour litige ou contentieux – est une procédure utilisée par les tribunaux fédéraux dans laquelle des affaires civiles impliquant des problèmes similaires et provenant de tout le pays sont consolidées et déplacées vers un seul tribunal.
Mise à jour février 2023
- 9 février 2023 : Mardi, Merck a déposé une requête demandant au juge du MDL de rejeter toutes les plaintes déposées à son encontre sur la base de théories délictuelles fondées sur un « défaut de conception ». Le National Childhood Vaccine Injury Act exclut expressément les plaintes pour défaut de conception à l’encontre des fabricants de vaccins et oblige les demandeurs à passer par une procédure administrative connue sous le nom de « tribunal des vaccins ». La requête de Merck soutient que la plupart des plaintes en responsabilité du fait des produits déposées par les plaignants du MDL sont de facto des plaintes pour défaut de conception, même s’ils évitent d’utiliser cette expression. Si cette requête est acceptée, elle réduira considérablement le champ d’application du litige Gardasil.
- 1er février 2023 : La semaine dernière, Merck a déposé un démenti et une liste de défenses affirmatives (denial and list of affirmative defenses, ), qui offre un aperçu détaillé de sa stratégie apparente pour défendre les actions en justice concernant le Gardasil. Merck soutiendra que les plaintes contre Gardasil fondées sur le défaut de mise en garde sont irrecevables en vertu de la loi nationale sur les vaccins pour enfants de 1986 (42 U.S.C. § 300aa-22). Merck a également l’intention de contester les allégations selon lesquelles Gardasil était « défectueux » dans sa conception et d’invoquer la défense de l’intermédiaire averti, qui fait peser sur les médecins l’obligation de mettre en garde contre les risques de Gardasil. Les avocats de Gardasil sont optimistes quant à la possibilité de faire échec à ces moyens de défense.
Mise à jour janvier 2023
- 18 janvier 2023 : Il y a maintenant 60 procès Gardasil en cours dans le cadre de l’action collective Gardasil MDL dans le district occidental de Caroline du Nord. Le recours collectif MDL a été créé en septembre avec un peu plus de 20 cas, ce qui signifie qu’il a déjà triplé. Il est probable qu’un afflux important de nouvelles affaires se produira prochainement, à mesure que les plaintes déjà déposées pour Gardasil seront traitées par le tribunal des vaccins.
- 12 janvier 2023 : En novembre, les plaignants du recours collectif Gardasil MDL ont déposé une requête visant à contraindre le défendeur, Merck & Co, à produire des documents supplémentaires et à compléter leurs réponses aux interrogatoires. Après avoir obtenu un délai supplémentaire pour répondre à cette requête, Merck et ses avocats ont maintenant jusqu’à la fin de cette semaine (5 janvier 2023) pour déposer une réponse à la requête (ou fournir des réponses supplémentaires à l’interrogatoire).
Mise à jour décembre 2022
La route vers le premier procès Gardasil est longue. Mais les avocats des victimes se rapprochent à mesure que l’on approche de 2023. L’obtention d’une date de procès est importante car un accord sur le Gardasil sera impossible sans une réelle pression sur les accusés. Les procès exercent une pression qui conduit à des accords.
Une proposition commune de programme bellwether (NdT : les procès Bellwether ont lieu lorsque de nombreux plaignants intentent des procès contre la même partie ou le même groupe de parties) a été soumise la semaine dernière par les avocats des deux parties au recours collectif Gardasil. Cette proposition conjointe prévoit la constitution d’un groupe de 16 dossiers, candidats à un procès au cours de l’année prochaine. Dans le cadre du plan de préparation au procès, six de ces affaires seraient sélectionnées pour le procès bellwether initial, et ces sélections seraient faites en août 2024. Le juge du MDL, Robert Conrad, approuvera et adoptera probablement le plan lors de la prochaine conférence mensuelle sur l’état d’avancement des travaux.
Mise à jour octobre 2022
La première conférence sur le statut du nouveau MDL Gardasil est prévue pour le 11 octobre devant le juge Robert Conrad, dans le district ouest de Caroline du Nord. L’un des principaux points à l’ordre du jour du juge Conrad sera la sélection des avocats qui feront partie du comité de direction des plaignants et la désignation de l’avocat principal. Le comité de direction est le groupe d’avocats qui prendra les décisions stratégiques pour tous les plaignants dans le cadre du litige.
Mise à jour août 2022
Le Panel MDL entendra les arguments visant à déterminer si les actions en justice relatives au vaccin Gardasil doivent être regroupées dans un recours collectif MDL. Les plaignants cherchent à obtenir une consolidation devant les tribunaux fédéraux de l’Arizona ou du Wisconsin, et Merck s’oppose à une action collective parce qu’elle estime que ces affaires devraient être portées devant un tribunal spécialisé dans les vaccins. L’audience du Panel MDL est prévue pour le 28 juillet 2022.
Mise à jour juin 2022
Le mois dernier, le JPML a accepté une requête visant à consolider tous les procès relatifs au vaccin Gardasil contre le papillomavirus dans un nouveau recours collectif. La nouvelle action collective – désignée sous le nom de In re : Gardasil Prod. Liab. Lit., MDL No. 3036 – a été confiée au juge Robert Conrad Jr. dans le district occidental de Caroline du Nord.
En acceptant la requête et en formant le nouveau MDL, le JPML a rejeté les arguments du défendeur Merck selon lesquels la consolidation du MDL serait en conflit avec le Vaccine Act et conduirait à l’hésitation face aux vaccins. Une conférence devant le juge aura lieu à Charlotte, en Caroline du Nord, en octobre 2022. La première conférence initiale dans le cadre de la nouvelle class action MDL Gardasil se concentrera sur la sélection des avocats qui feront partie du comité de direction ou de pilotage des plaignants.
Ce comité est composé d’avocats représentant les plaignants dans le MDL Gardasil. Les avocats des plaignants ont initialement montré peu d’intérêt pour le procès Gardasil, mais la certification de l’action collective contribuera à sensibiliser certains avocats à la viabilité de ces procès. Il sera donc intéressant de voir quels avocats poseront leur candidature au comité de pilotage.
Le comité est chargé de prendre des décisions pour tous les autres plaignants du Gardasil. La conférence abordera également d’autres questions administratives, telles que la création de formulaires de plaidoirie et d’un plan de communication de pièces – en d’autres termes, comment donner le coup d’envoi à ce litige.
Qu’est-ce que le HPV ?
Le papillomavirus humain (HPV pour Human Papillomavirus)) est une infection virale qui se transmet par contact cutané, en particulier par contact sexuel. Il existe plus de 200 souches d’HPV, dont plus de 40 peuvent être transmises par voie sexuelle.
Le papillomavirus est la maladie sexuellement transmissible la plus courante et on estime que la majorité des personnes sexuellement actives le contracteront un jour ou l’autre. Toutefois, plus de 90 % des infections à HPV ne provoquent aucun symptôme clinique et sont éliminées naturellement par le système immunitaire de l’organisme. Seul un nombre limité de souches de HPV, environ 12 à 18, est lié au cancer du col de l’utérus.
Les infections persistantes par ces souches peuvent provoquer des lésions précancéreuses, qui peuvent être détectées par frottis et éliminées. Le tabagisme et d’autres facteurs peuvent également augmenter le risque de cancer du col de l’utérus.
Le test Pap (NdT : test Papanicolaou, test à partir d’un frotti) est la réponse de santé publique de première ligne la plus efficace contre la maladie et a permis de réduire les taux de cancer du col de l’utérus dans les pays développés jusqu’à 80 %. Le cancer du col de l’utérus est dans une large mesure traitable, avec un taux de survie à cinq ans de plus de 90 % lorsqu’il est détecté à un stade précoce. Merck a cherché à accélérer la mise sur le marché d’un vaccin destiné à prévenir l’infection par quatre types d’HPV, mais seules deux de ces souches sont associées au cancer.
Poursuites judiciaires concernant le vaccin HPV Gardasil
Gardasil® est un vaccin mis au point par Merck & Co. pour prévenir le HPV (papillomavirus humain). Merck a obtenu l’approbation du Gardasil en 2006 grâce à des essais de recherche trompeurs, qui ont exagéré les avantages et largement sous-estimé les risques et les effets secondaires du vaccin. Merck a commercialisé le Gardasil de manière agressive en utilisant des tactiques de peur, de la publicité mensongère et des lobbyistes politiques pour inciter des millions de parents à vacciner leurs adolescentes avec le Gardasil.
Aujourd’hui, des milliers de jeunes filles ayant reçu le vaccin Gardasil subissent de graves conséquences sur leur santé, et des centaines d’entre elles sont décédées à la suite de complications liées au vaccin. Notre cabinet est actuellement à la recherche de nouveaux cas de Gardasil. Si vous avez reçu le vaccin Gardasil contre le papillomavirus et que vous avez par la suite subi des effets secondaires, des complications ou d’autres événements indésirables pouvant être liés au vaccin, appelez-nous dès aujourd’hui au 800-553-8082 pour une consultation gratuite afin de discuter de ce qu’un procès Gardasil pourrait faire pour vous.
Approbation du vaccin Gardasil
Gardasil est un vaccin censé protéger contre le HPV. Le HPV est une infection virale très répandue qui se transmet par contact cutané. Le HPV est la maladie sexuellement transmissible la plus courante, et la majorité des personnes contracteront le HPV à un moment ou à un autre de leur vie. La plupart des cas de HPV sont bénins, mais s’ils ne sont pas traités, un très faible pourcentage de cas de HPV chez les femmes peut évoluer vers un cancer du col de l’utérus.

Merck a obtenu une autorisation accélérée de la FDA pour Gardasil en juin 2006. À l’époque, Merck était encore sous le choc des pertes d’un milliard de dollars encourues après avoir été contraint de retirer son médicament Vioxx du marché. Au sein de Merck, Gardasil était décrit comme le « Saint Graal » qui aiderait l’entreprise à remplacer les revenus perdus à cause du Vioxx. Les cadres de Merck disaient souvent que « HPV » signifiait « Help Pay for Vioxx » (aide à payer pour le Vioxx).
Au cours de la procédure d’approbation accélérée, Merck a dissimulé des faits importants concernant l’efficacité (ou l’absence d’efficacité) et la sécurité de Gardasil. Merck n’a pas effectué d’investigations et d’études médicales complètes et appropriées au cours des phases de préapprobation ou de post-approbation.
Les essais cliniques entrepris par Merck n’ont même pas examiné le potentiel de Gardasil à prévenir le cancer, mais ont seulement analysé si Gardasil pouvait prévenir des conditions précurseurs potentielles. Merck a ensuite présenté des données trompeuses suggérant que ces « conditions précurseurs » aboutissent inexorablement à un cancer.
La campagne de marketing mensongère de Merck pour promouvoir le Gardasil
Avant et après l’approbation du Gardasil, Merck s’est livrée à des tactiques de marketing peu scrupuleuses visant à exagérer les risques associés au HPV et la prétendue efficacité du Gardasil afin d’effrayer le public et de l’amener à accepter des vaccinations massives avec le vaccin Gardasil.
Avant Gardasil, il n’y avait pas d’urgence de santé publique liée au HPV aux États-Unis et peu de femmes avaient entendu parler du HPV, de sorte que la demande de vaccin contre le HPV était faible, voire inexistante. Pour garantir le succès financier de son nouveau « Saint-Graal », Merck a précédé le lancement du Gardasil par des années de marketing coûteux de « sensibilisation à la maladie » du papillomavirus.
Une fois que Gardasil a été autorisé pour les préadolescentes, Merck a lancé une campagne de propagande agressive visant à effrayer et à culpabiliser les parents qui n’avaient pas vacciné leurs filles avec Gardasil. La campagne de Merck impliquait que les « bons parents » vaccinent leurs enfants avec Gardasil.
Au cours de ces efforts de marketing agressifs, Merck a frauduleusement dissimulé les risques et les dangers connus du vaccin anti-HPV tout en exagérant son efficacité. Merck a commercialisé le Gardasil avec la campagne la plus agressive jamais organisée pour promouvoir un vaccin, en dépensant plus pour la publicité du Gardasil que pour toute autre campagne publicitaire antérieure sur les vaccins.
Implications dans la vie réelle de la soif de profits de Merck
Le lobbying politique de Merck pour rendre le Gardasil obligatoire
Outre sa campagne publicitaire agressive, Merck a également eu recours à des lobbyistes politiques et à des incitations financières pour amener les assemblées législatives des États à rendre le vaccin Gardasil obligatoire pour tous les enfants scolarisés. À partir de 2004, Merck a injecté des millions dans des organisations de lobbying politique telles que ‘Les Femmes dans le Gouvernement’ ( Women in Government ) et NACCHO. Ces organisations ont alors commencé à faire pression de manière agressive sur les législateurs du pays ( pushing legislators ) pour qu’ils rendent obligatoires les vaccins Gardasil pour toutes les filles de 6ème (NdT : 11 à 12 ans).
Merck a complété ces lobbyistes rémunérés par des contributions à des campagnes politiques et des millions de dollars de financement direct aux départements de santé des États. Entre 2012 et 2018, Merck a versé directement 92 millions de dollars au ministère de la santé du Maryland pour la promotion des vaccins Gardasil dans les écoles publiques. Ce financement a essentiellement permis de payer les responsables des écoles pour qu’ils trompent les élèves et les parents en leur faisant croire (deceive students and parents ) que la vaccination par Gardasil était obligatoire.
Merck a présenté de manière erronée l’efficacité de Gardasil
Pour convaincre les organismes de réglementation et les responsables de la santé publique d’accepter le Gardasil, les poursuites judiciaires relatives au Gardasil allèguent que Merck a présenté de manière erronée l’efficacité du vaccin en annonçant faussement que le Gardasil prévient le cancer du col de l’utérus. Aucune étude crédible ne démontre que Gardasil prévient le cancer du col de l’utérus.
Merck n’a pas voulu investir le temps et l’argent nécessaires pour effectuer des tests qui prouveraient que son vaccin prévient le cancer du col de l’utérus. Au lieu de cela, Merck a persuadé les autorités réglementaires de l’autoriser à utiliser des « critères de substitution » pour étayer sa théorie selon laquelle les vaccins anti-HPV seraient efficaces pour prévenir le cancer du col de l’utérus. L’utilisation de ces critères de substitution a permis à Merck de raccourcir les essais cliniques à quelques années et d’obtenir l’approbation réglementaire des vaccins sans aucune preuve que les vaccins préviendraient le cancer à long terme.
En janvier 2020, une étude britannique a soulevé des doutes importants quant à la prévention du cancer du col de l’utérus par le vaccin Gardasil, comme le prétendait Merck. L’étude souligne le fait qu’il n’a jamais été prouvé que le Gardasil prévenait le cancer du col de l’utérus (ou tout autre type de cancer).
Gardasil pourrait AUGMENTER le risque de cancer du col de l’utérus
Contrairement aux affirmations de Merck, le Gardasil pourrait augmenter le risque de cancer du col de l’utérus et d’autres cancers, et non les prévenir. Plusieurs études (dont une du CDC qui, jusqu’à présent, a toujours soutenu le vaccin) ont montré qu’en supprimant certaines souches de HPV, les vaccins Gardasil peuvent favoriser des changements mutagènes dans le virus qui peuvent conduire au cancer.
Les données de santé publique semblent étayer la conclusion selon laquelle le Gardasil pourrait augmenter le taux de cancer du col de l’utérus. Après l’introduction du vaccin contre le HPV en Grande-Bretagne, les taux de cancer du col de l’utérus chez les jeunes femmes âgées de 25 à 29 ans ont augmenté de 54 %.
En Australie, 13 ans après la mise sur le marché du Gardasil et sa diffusion auprès des adolescents, il y a eu une augmentation de 16 % chez les femmes de 25 à 29 ans et de 30 % chez les femmes de 30 à 34 ans. Parallèlement, les taux diminuent chez les femmes plus âgées (qui n’ont pas été vaccinées).
En d’autres termes, le Gardasil peut augmenter le risque de cancer. C’est ce qui constituera l’essentiel de la demande pour certaines victimes qui intentent un procès contre le vaccin Gardasil. Mais il reste encore des recherches à faire sur cette question.
Pour la plupart des femmes qui intentent un procès contre le Gardasil pour effets secondaires à long terme ou troubles auto-immuns, l’accent ne sera pas mis de savoir si le Gardasil aide à prévenir le cancer du col de l’utérus. L’accent sera mis sur l’autre effet secondaire que le Gardasil peut provoquer et auquel les gens, principalement les filles, ne s’attendaient pas lorsqu’elles ont reçu le vaccin contre le HPV.
Les effets secondaires à long terme et troubles auto-immuns du Gardasil HPV
Des recherches scientifiques récentes ont montré que le Gardasil induit et augmente le risque de nombreux effets secondaires à long terme liés à des troubles auto-immuns. Plus précisément, le Gardasil a été associé aux maladies auto-immunes suivantes :
- syndrome de Guillain-Barré
- syndrome de tachycardie orthostatique posturale
- polyneuropathie inflammatoire démyélinisante chronique
- sclérose en plaques
Le Gardasil a également été associé à une myriade d’effets secondaires à long terme liés à des maladies auto-immunes induites, y compris des dangers tels que la fibromyalgie, la dysautonomie, l’insuffisance ovarienne prématurée, le syndrome de fatigue chronique et le syndrome de douleur régionale chronique, des migraines, des maux de tête sévères, des malaises gastro-intestinaux persistants, des douleurs généralisées à caractère neuropathique, le syndrome d’encéphalite, des dysfonctionnements autonomes, des douleurs articulaires et un brouillard cérébral.
Divers articles publiés dans des revues médicales ont discuté de l’association entre le Gardasil et une myriade de lésions graves et ont fait état de patientes développant un POTS (NdT : Postural Orthostatic Tachycardia – syndrome de tachycardie orthostatique posturale, trouble de la circulation sanguine), une IO (NdT : Osteogenesis imperfecta,- Ostéogénèse Imparfaite, fragilité des os) une fibromyalgie et d’autres symptômes de déficience autonome des années plus tard après avoir été vaccinées par le Gardasil. Notre cabinet se concentre sur les demandes d’indemnisation pour insuffisance ovarienne prématurée.
Le Gardasil lié à une insuffisance ovarienne prématurée
L’insuffisance ovarienne prématurée est l’un des effets secondaires les plus graves pouvant être provoqués par le vaccin Gardasil contre le papillomavirus. L’insuffisance ovarienne prématurée (également appelée insuffisance ovarienne primaire) survient lorsque les ovaires cessent de fonctionner et de produire des ovules avant l’âge de 40 ans et avant la ménopause.
L’insuffisance ovarienne prématurée est associée à une production anormale d’œstrogènes dans les ovaires. L’insuffisance ovarienne prématurée est une affection grave car elle peut entraîner la stérilité. De nombreux facteurs peuvent entraîner une insuffisance ovarienne prématurée, tels qu’une défaillance auto-immune, des anomalies du chromosome X, des causes idiopathiques, des toxines et, bien sûr, l’ablation des ovaires.
Plusieurs études médicales récentes ont révélé que l’insuffisance ovarienne prématurée peut être déclenchée par une réaction auto-immune au vaccin Gardasil HPV. Cette réaction se produit lorsque le système immunitaire de l’organisme produit des anticorps qui attaquent le tissu des ovaires qui contient les ovules.
La première étude importante établissant un lien entre l’insuffisance ovarienne prématurée et le vaccin Gardasil a été publiée en 2020 et a identifié un nombre disproportionné de rapports d’événements indésirables liés au vaccin impliquant une insuffisance ovarienne prématurée et une ménopause prématurée. Une étude de suivi a été publiée (published ) en mars 2022 dans la revue Drugs Real World Outcomes (NdT : c’est le NIH – National Institute of Health, l’Institut National de la Santé qui a publié dans la National Library of Health, Bibliothèque Nationale de la Santé). Cette étude a également conclu à l’existence d’un lien potentiel entre l’insuffisance ovarienne prématurée et le vaccin contre le papillomavirus.
- Étude de (Case study ) cas sur le lien entre l’insuffisance ovarienne prématurée et le vaccin contre le HPV.
Poursuites judiciaires Gardasil
L’émergence de preuves récentes établissant un lien entre le Gardasil et divers troubles auto-immuns et autres problèmes de santé a donné lieu à des poursuites en responsabilité du fait des produits Gardasil à l’encontre de Merck. Ces procès sont intentés par des femmes qui ont développé une maladie auto-immune et d’autres problèmes de santé graves tels que le syndrome de tachycardie orthostatique (POTS).
Les actions en justice contre Gardasil accusent Merck d’avoir dissimulé frauduleusement des preuves concernant les risques pour la santé du Gardasil tout en le présentant faussement comme un vaccin capable de prévenir le cancer du col de l’utérus. Les plaintes contre Merck dans le cadre d’un procès Gardasil comprennent les plaintes traditionnelles en responsabilité civile du fait des produits, telles que le défaut de mise en garde, le défaut de fabrication et la négligence.
Le recours collectif contre Gardasil comprend également des plaintes pour fraude. Ces dernières sont moins courantes dans les procès en responsabilité du fait des produits, soulignant à quel point les avocats de Gardasil se sentent à propos de la conduite de Merck.
Peu d’avocats spécialisés dans le Gardasil demandent un rappel du Gardasil. Il est important de comprendre cela pour apprécier ce qu’un procès Gardasil cherche à obtenir. Ce n’est pas que le Gardasil soit déraisonnable pour tout le monde, et c’est pourquoi il n’y a pas de vague de fond en faveur d’un rappel. Le problème est que les patients, les médecins et les parents auraient dû recevoir des informations précises sur les avantages et les effets secondaires du Gardasil.
Notre cabinet recherche actuellement de nouveaux cas Gardasil pour toute personne ayant reçu le vaccin Gardasil et ayant été diagnostiquée par la suite avec des troubles auto-immuns tels que des maladies auto-immunes et d’autres problèmes de santé graves tels que le le syndrome de tachycardie orthostatique (POTS) ou l’un des problèmes de santé connexes suivants :
| Syndrome de Guillain–Barré | Intolérance orthostatique |
| Neuropathie à petites fibres | Polyneuropathie inflammatoire démyélinisante chronique |
| Lupus érythémateux disséminé | Sclérose en plaques |
| Pancréatite auto-immune | Hépatite auto-immune |
| Fibromyalgie | Insuffisance ovarienne précoce |
| Syndrome douloureux régional chronique |
Le procès Gardasil et la loi sur les vaccins
En mars 2022, un juge fédéral du Nevada a rejeté une action en justice concernant le Gardasil au motif qu’elle était « partiellement » exclue du champ d’application de la loi sur les vaccins (Vaccine Act). La loi sur les vaccins est une loi fédérale qui interdit les plaintes pour défaut de conception et certaines plaintes pour défaut de mise en garde à l’encontre des fabricants de vaccins, mais qui autorise les plaintes pour négligence.
Dans l’affaire Flores v. Merck & Co, la plaignante allègue qu’après avoir reçu le vaccin Gardasil contre le papillomavirus, son corps s’est effondré. Elle a souffert de vertiges, de fatigue et de nausées, et ces symptômes se sont progressivement aggravés au fil du temps.
Merck a déposé une requête en irrecevabilité fondée sur la loi nationale sur les blessures causées par les vaccins aux enfants (National Childhood Vaccine Injury Act – NCVIA). Qu’est-ce que la loi sur les vaccins ? La loi sur les vaccins est une loi adoptée en 1986 qui a créé un programme d’indemnisation sans égard à la faute pour les lésions causées par les vaccins chez les enfants.
Le tribunal a convenu avec Merck que la plainte pour négligence du plaignant était une plainte pour défaut de conception « mal déguisée » et, par conséquent, interdite par la loi sur les vaccins. Le tribunal a également estimé que l’action pour défaut de mise en garde, telle qu’elle était formulée dans le procès Gardasil du demandeur, semblait être exclue par la loi sur les vaccins et devait être rejetée.
Bien que le juge ait finalement rejeté toutes les demandes de la plaignante, la plupart des rejets étaient « sans préjudice », ce qui signifie que la plaignante a la possibilité de « réessayer » en réécrivant ses demandes et en déposant une plainte modifiée.
Le procès Gardasil n’est donc pas mort. Mais une plainte modifiée doit préciser que la plainte pour négligence n’est pas une plainte pour défaut de conception. En ce qui concerne la plainte pour défaut de mise en garde, la plainte modifiée doit simplement clarifier les allégations selon lesquelles Merck n’a pas mis en garde les prestataires médicaux du plaignant contre les risques spécifiques associés au vaccin Gardasil. Une plainte modifiée a été déposée. Et, oui, Merck a déposé une nouvelle requête en irrecevabilité.
Mais la loi sur les vaccins constitue un problème pour ceux qui souhaitent intenter un procès contre Gardasil. Chaque avocat de Gardasil doit trouver un moyen de contourner la loi. Dans le cas contraire, l’action en justice relative à Gardasil sera jugée irrecevable, ce qui obligera la victime à demander une indemnisation au titre du programme national d’indemnisation des victimes de vaccins (National Vaccine Injury Compensation Program). Ces indemnités seront bien inférieures à celles que les jurés accorderaient dans le cadre d’un procès civil s’ils croyaient en la plainte de la victime.
Contactez-nous au sujet d’un procès concernant le vaccin HPV Gardasil
Si vous pensez avoir développé une maladie auto-immune ou un autre problème de santé à cause d’un vaccin HPV Gardasil, vous devriez envisager de porter plainte dans un recours contre Gardasil afin d’obtenir un verdict ou un règlement équitable pour les dommages que vous avez subis. Appelez un avocat spécialiste Gardasil dès aujourd’hui pour une consultation gratuite au 800-553-8082 ou obtenez une consultation gratuite en ligne free online consultation.
Observation à long terme des effets indésirables possibles chez les adolescentes japonaises après la vaccination contre le papillomavirus humain
[Source de l’étude : ncbi.nlm.nih.gov]
Par – Akiyo Hineno1,2 and Shu-Ichi Ikeda1,3,* – Gloria Calagna, Academic Editor
Résumé
Au Japon, un nombre important d’adolescentes ont présenté des symptômes inhabituels après avoir été vaccinées contre le virus du papillome humain (HPV). La grande majorité d’entre elles ont d’abord été diagnostiquées comme souffrant de maladies psychiatriques en raison de l’absence d’images radiologiques pathologiques et d’anomalies spécifiques dans les résultats des tests de laboratoire. Par la suite, ces symptômes ont été considérés comme des effets indésirables de la vaccination contre le papillomavirus. Cependant, un lien de causalité entre la vaccination contre le HPV et l’apparition de ces symptômes n’a pas été démontré. Entre juin 2013 et mars 2021, nous avons examiné 200 patients ayant présenté divers symptômes après la vaccination contre le HPV. Au total, 87 d’entre eux ont été diagnostiqués comme présentant des symptômes liés à la vaccination contre le HPV sur la base des critères diagnostiques que nous avons proposés. Les antécédents cliniques de ces 87 patients ont été analysés. L’âge au moment de la première vaccination allait de 11 à 19 ans (moyenne ± écart-type : 13,5 ± 1,5 ans), et l’âge au moment de la première apparition des symptômes allait de 12 à 20 ans (moyenne ± écart-type : 14,3 ± 1,6 ans). Les patients ont reçu une première injection de vaccin anti-HPV entre mai 2010 et mai 2013, mais le premier patient affecté a développé des symptômes en octobre 2010, et le dernier a développé des symptômes en octobre 2015. Un groupe de patients atteints d’un trouble post-vaccination contre le HPV n’est pas apparu au Japon au cours des cinq dernières années. Notre étude montre qu’au Japon, la période de vaccination contre le HPV a considérablement chevauché celle du développement d’un trouble post-vaccination contre le HPV unique en son genre. Ce trouble apparaît comme une combinaison d’intolérance orthostatique, de syndrome douloureux régional chronique et de dysfonctionnement cognitif, mais sa pathogénie exacte reste incertaine.
1. Introduction
L’infection par le papillomavirus humain (HPV) joue un rôle crucial dans le développement des cancers du col de l’utérus (1). C’est pourquoi, en mai 2010, les vaccins contre le HPV, Cervarix® (GlaxoSmithKline, Brentford, UK), un vaccin bivalent recombinant contre le papillomavirus, et Gardasil® (Merck & Co, Inc., Kenilworth, NJ, USA), un vaccin quadrivalent recombinant contre le papillomavirus, ont été largement introduits chez les adolescentes japonaises (2,3). Depuis avril 2013, les adolescentes âgées de 13 à 16 ans sont légalement tenues de se faire vacciner. Peu de temps après le début de ce programme de vaccination, un nombre important de jeunes filles vaccinées se sont plaintes d’un trouble unique composé de mouvements involontaires violents et tremblants, de douleurs chroniques et de faiblesses dans les membres. Les médias japonais ont largement rapporté qu’une combinaison de ces symptômes n’avait jamais été observée auparavant, suggérant que ce trouble était une réaction indésirable possible à la vaccination contre le papillomavirus. Les présentations répétées à la télévision de femmes vaccinées souffrantes ont eu un fort impact sur la société japonaise, forçant le ministère japonais de la santé publique, du travail et de la protection sociale à retirer la recommandation de vaccination contre le HPV à la fin du mois de juin 2013 (4). Simultanément, un comité spécial a été mis en place pour enquêter sur les femmes japonaises affectées, et notre institution a été l’un des centres d’enquête au cours des huit dernières années.
Dans nos deux rapports précédents (5,6), nous avons décrit les caractéristiques cliniques et les critères de diagnostic des femmes japonaises concernées par le trouble post-vaccination contre le papillomavirus. Ce trouble semble inclure une dysrégulation orthostatique, un syndrome douloureux régional chronique (SDRC) et un dysfonctionnement cognitif (5,6,7). Les réactions auto-immunes anormales post-vaccinales sont supposées être responsables de ce trouble (8,9 ), mais aucun lien de cause à effet n’a été établi entre la vaccination contre le HPV et l’apparition de ces symptômes. C’est pourquoi, dans cette étude, nous avons tenté de clarifier la relation temporelle entre la vaccination contre le HPV et le développement de cette maladie particulière, en nous basant sur l’observation à long terme des femmes japonaises touchées, effectuée par notre centre unique.
2. Matériels et méthodes
Entre juin 2013 et mars 2021, nous avons examiné les symptômes et les résultats objectifs de 200 patientes vaccinées contre le HPV. Conformément aux critères diagnostiques que nous avons proposés (6 ), nous avons recueilli les informations nécessaires sur les patientes, en accordant une attention particulière à la durée écoulée entre la vaccination et l’apparition des premiers symptômes soupçonnés d’être liés au vaccin. Les patientes ont subi des examens physiques et neurologiques ainsi que des tests de laboratoire de routine. La température de la peau et un pléthysmogramme numérique ont été enregistrés et, si nécessaire, le test de Schellong a été effectué. En outre, des tests neuropsychologiques et une imagerie cérébrale fonctionnelle ont été réalisés chez les patientes présentant un dysfonctionnement cognitif. Les détails de ces méthodes sont décrits dans nos rapports précédents (5,6). Le protocole de l’étude a été approuvé par l’Institutional Review Board – Comité d’Examen Institutionnel (approbation n° 4128 et 4150) de la Shinshu University School of Medicine, Matsumoto, Japon.
3. Résultats
Au cours des huit dernières années, 200 patientes ont consulté notre hôpital en raison d’une suspicion d’effets indésirables liés au vaccin contre le HPV (33 patientes en 2013, 43 en 2014, 38 en 2015, 49 en 2016, 25 en 2017, 8 en 2018, 4 en 2019, 0 en 2020, 0 en 2021). Parmi elles, nous avons exclu 19 patientes qui présentaient des symptômes avant la vaccination et 5 qui ont reçu le vaccin anti-HPV après l’âge de 30 ans. Nous avons également exclu 28 autres patientes dont les symptômes ou les troubles s’expliquaient par des maladies connues ou qui présentaient des données de laboratoire anormales, à savoir huit patientes atteints d’épilepsie, six patientes souffrant de troubles psychiatriques ou anxieux, trois patients atteints de lupus érythémateux disséminé, une patiente souffrant d’arthrite juvénile idiopathique, une patiente souffrant de polymyosite avec anticorps anti-SGPS et neuf patientes souffrant d’autres maladies. Pour les 148 patientes restantes, les manifestations cliniques et les résultats objectifs ont été analysés. Les résultats ont montré que 32 patientes ont été diagnostiquées avec des symptômes certains liés au vaccin, et 55 avec des symptômes probables liés au vaccin. Les symptômes et signes des 87 patientes diagnostiquées sont résumés dans le tableau 1 (Table 1). Le symptôme le plus fréquent était une fatigue générale prolongée, qui entraînait une incapacité à se réveiller et à aller à l’école le matin. Des céphalées sévères, des douleurs étendues aux membres et au tronc et des symptômes dysautonomiques, notamment des évanouissements orthostatiques et des dysfonctionnements intestinaux, étaient également à l’origine d’une diminution marquée de l’activité quotidienne des patientes. En outre, la douleur généralisée se manifestait typiquement par une douleur articulaire migratoire sans aucun signe d’inflammation, et une douleur névralgique intermittente dans la poitrine ou la paroi abdominale était fréquente. Le dysfonctionnement moteur présentait des schémas variables, mais la faiblesse dominante distale des membres, qui imitait celle de la polyneuropathie, était prédominante. Les sensations anormales étaient principalement observées au niveau des cuisses ou de la partie inférieure des jambes, où la dysesthésie ou l’allodynie étaient fréquentes. Par rapport à ces symptômes, les troubles de l’apprentissage et du sommeil sont apparus plus tardivement. Les patientes se sont plaintes d’un manque de clarté mentale. Les résultats objectifs fréquemment observés étaient une dysrégulation orthostatique, y compris le syndrome de tachycardie orthostatique posturale (POTS), des enregistrements anormaux du pléthysmogramme numérique et des anomalies sur les images SPECT du cerveau. Les détails de ces observations ont été décrits dans un rapport précédent (6).
Tableau 1
Fréquence des symptômes et des signes chez les 87 patientes étudiées.
| Symptômes | Nombre de cas | Fréquence (%) |
|---|---|---|
| Fatigue générale | 73 | 83.9 |
| Maux de tête intenses | 72 | 82.8 |
| Douleur généralisée | 71 | 81.6 |
| Symptômes dysautonomiques | 71 | 81.6 |
| Dysfonctionnement de la motricité | 56 | 64.4 |
| Sensations anormales | 52 | 59.8 |
| Troubles de l’apprentissage | 52 | 59.8 |
| Troubles du sommeil | 44 | 50.6 |
| Anomalies de la menstruation | 44 | 50.6 |
| Tremblement des membres | 41 | 47.1 |
La distribution temporelle de la période de vaccination initiale et de l’apparition du premier symptôme chez les 87 patients diagnostiqués est présentée dans la Figure 1. La période de vaccination initiale s’étend de mai 2010 à mai 2013, et l’âge au moment de la vaccination initiale varie de 11 à 19 ans (moyenne ± écart-type : 13,5 ± 1,5 ans). Par ailleurs, le premier symptôme est apparu entre octobre 2010 et octobre 2015, et l’âge d’apparition des premiers symptômes était compris entre 12 et 20 ans (moyenne ± écart-type : 14,3 ± 1,6 ans). Ainsi, le délai entre la première dose de vaccin et l’apparition des symptômes était compris entre 0 et 1532 jours (médiane : 199 jours). L’intervalle entre l’apparition des symptômes et notre premier examen allait de 0 à 85 mois (médiane : 31 mois), indiquant la durée de la maladie chez les patients avant qu’ils ne se rendent dans notre centre.
Figure 1 (ci-dessous)
Relation temporelle entre la vaccination contre le HPV et l’apparition de symptômes chez les patients diagnostiqués comme présentant des symptômes liés au vaccin contre le HPV. La période présentée ici s’étend de mai 2010 à mars 2021. (a) Nombre de patients ayant reçu la première injection du vaccin anti-HPV chaque mois. La flèche indique la date à laquelle le ministère japonais de la santé publique, du travail et des affaires sociales a cessé de recommander la vaccination contre le papillomavirus. (b) Nombre de patients ayant développé des symptômes chaque mois. (c) Nombre de patients qui ont consulté notre établissement et ont été diagnostiqués comme souffrant d’un trouble post-vaccination contre le HPV chaque mois.

La relation temporelle entre la vaccination contre le HPV et l’apparition des symptômes était la suivante : la première injection du vaccin contre le HPV a eu lieu en mai 2010 et la dernière en mai 2013 (Figure 1a). La première femme vaccinée affectée a développé des symptômes en octobre 2010, et la dernière apparition des symptômes a eu lieu chez deux patientes en octobre 2015 ; la période de pointe de la première injection du vaccin anti-HPV semble se situer entre juillet 2011 et septembre 2012, et celle du développement de symptômes post-vaccinaux uniques est apparue entre septembre 2011 et août 2013 (Figure 1a,b). Au cours des cinq années précédentes, nous n’avons examiné aucune patiente nouvellement affectée par ces symptômes uniques (Figure 1b).
4. Discussion
L’innocuité du vaccin anti-HPV a été rapportée dans les pays où la vaccination anti-HPV est prédominante (10,11,12 )En Australie notamment, bien qu’une syncope se produise parfois après la vaccination HPV, la fréquence d’autres effets indésirables graves, notamment le syndrome post-traumatique, le syndrome de fatigue chronique, l’insuffisance ovarienne primaire, le syndrome de Guillain-Barré, les maladies auto-immunes et la thrombose veineuse, est très faible, ce qui suggère qu’il n’y a pas de lien de cause à effet (13 ). Cependant, le risque potentiel de vaccination contre le HPV et de dysautonomie, de CRPS ( Complex regional pain syndrome – syndrome douloureux régional complexe (SDRC) est un terme général décrivant une douleur et une inflammation excessives et prolongées) et de syndrome de fatigue chronique a été identifié sur la base d’une série de rapports de cas provenant de différents pays (14,15,16,17,18,19). Les questions de sécurité concernant les vaccins contre le papillomavirus restent donc controversées (20).
Selon les rapports d’un comité spécial japonais(21,22), 3,39 millions de Japonaises ont été vaccinées contre le papillomavirus entre mai 2010 et novembre 2016, et 2024 personnes ont été signalées comme ayant des effets indésirables, dont 673 ont présenté des symptômes graves. Cependant, l’incidence des effets indésirables au cours de cette période de vaccination a été jugée faible et non significative, même si des symptômes similaires n’ont pas été observés à la suite d’autres vaccins.
Les manifestations cliniques variables des troubles post-vaccination contre le HPV peuvent s’expliquer par une combinaison de dysrégulation orthostatique, se manifestant principalement sous la forme d’un syndrome de stress post-traumatique (POTS), de syndrome douloureux régional complexe (NdT : voir ci-dessus CRPS) et/ou d’un dysfonctionnement cognitif (5,6,23). Des recherches récentes ont montré que parmi le POTS, le SDRC et l’encéphalomyélite myalgique/fatigue chronique (EM/SFC), certaines conditions se chevauchent (24,25,26) ; en particulier pour le dysfonctionnement cognitif, la lenteur de la pensée, la difficulté à se concentrer, le manque de concentration, l’oubli et la confusion sont couramment observés dans les trois troubles et correspondent à un flou dans le processus de pensée, que l’on appelle actuellement « brouillard cérébral » (27). Ainsi, le dysfonctionnement cognitif observé chez les patients souffrant de troubles post-vaccination contre le HPV pourrait être un état pathologique induit secondairement par le POTS et/ou le CRPS de longue durée. En outre, le SOPT, le CRPS et l’EM/SFC semblent présenter des anomalies auto-immunes similaires (28) , et quelques études préliminaires (29,30,31,32,33 ) et rapports de cas (34,35,36,37) ont montré que la présence d’auto-anticorps sériques contre les récepteurs des nerfs autonomes pourrait être un facteur déterminant dans la pathogenèse de ces trois troubles. En relation avec cette hypothèse, nous avons étudié les auto-anticorps dirigés contre les récepteurs des nerfs autonomes dans le sérum des patients atteints et avons révélé que les taux sériques d’auto-anticorps dirigés contre les récepteurs adrénergiques et les récepteurs muscariniques de l’acétylcholine étaient significativement plus élevés chez les patients vaccinés contre le papillomavirus que chez les témoins (38). Cependant, il n’y avait pas d’association statistiquement significative entre les symptômes cliniques et les taux sériques élevés de ces auto-anticorps. D’autres études sont donc nécessaires pour envisager la possibilité de réactions auto-immunes anormales liées à la vaccination contre le HPV.
Dans notre rapport précédent (6), nous avons décrit une relation temporelle étroite entre l’administration du vaccin HPV et l’apparition d’éventuels symptômes indésirables chez 72 patients japonais, sur la base d’une observation de quatre ans. Dans la présente étude, nous avons étendu cette période d’observation à près de huit ans et le nombre de patients diagnostiqués est passé à 87, réaffirmant que la période de vaccination contre le papillomavirus s’est considérablement chevauchée avec celle du développement d’un trouble post-vaccinal unique dans notre pays. Au Japon, la couverture vaccinale contre le papillomavirus des jeunes filles âgées de 12 à 16 ans est tombée à moins de 1 % après l’abandon de la recommandation gouvernementale (39), et au cours des trois dernières années, peu de jeunes filles sont venues nous voir pour des évaluations concernant un trouble post-vaccinal présumé lié au papillomavirus. Ces observations indiquent que les injections intensives de vaccins anti-HPV entre mai 2010 et mai 2013 ont induit un groupe de patientes japonaises présentant un trouble post-vaccination anti-HPV unique. Le Japon n’est pas le seul pays exceptionnel où le taux de vaccination contre le HPV a été extrêmement bas au cours des dernières années ; des pays d’Amérique latine, comme la Colombie, ont suivi un schéma similaire (40 ). Les réactions indésirables aux vaccins HPV semblent être influencées par différents contextes génétiques, culturels et/ou religieux. Ces affections, qui ne s’accompagnent pas d’images radiologiques ou de données de laboratoire anormales, sont souvent difficiles à diagnostiquer, ce qui conduit facilement au piège du diagnostic de maladie psychiatrique.
Néanmoins, s’il est possible que des effets indésirables surviennent après la vaccination contre le HPV, ces résultats ne signifient pas nécessairement que l’utilité de ce vaccin pour la prévention du cancer du col de l’utérus est remise en question (41). Si les informations rapportées dans cette étude sont fournies et largement disponibles lors de l’introduction des vaccins HPV, il est probable qu’il n’y aura pas de désapprobation sociale pour la vaccination anti-papillomavirus (All Japan Coordinating Association of HPV Sufferers – Association japonaise de coordination des malades du papillomavirus) au Japon. Les vaccins contre le papillomavirus sont prophylactiques et non thérapeutiques, et les effets indésirables graves ne sont donc pas acceptables, même si leur incidence est faible. Une surveillance étendue et une discussion ouverte sont recommandées pour garantir la sécurité de l’annonce des vaccins HPV (42).
Contributions des auteurs
Conceptualisation, A.H. et S.-I.I. ; conception de cette étude, A.H. et S.-I.I. ; analyse des données, A.H. ; rédaction du manuscrit, A.H. et S.-I.I. Les deux auteurs ont lu et approuvé la version publiée du manuscrit.
Financement (NdT : Financement de l’étude)
Ce travail a bénéficié d’une subvention du Ministère Japonais de la Santé Publique, du Travail et des Affaires Sociales pour la recherche sur les maladies infectieuses émergentes et ré-émergentes (Mise en place d’un système de diagnostic et de traitement des symptômes après la vaccination contre le papillomavirus, n° de subvention 19HA1006) accordée à S.-I.I.
Déclaration du comité d’examen institutionnel
L’étude a été menée conformément aux directives de la Déclaration d’Helsinki et approuvée par le comité d’examen institutionnel (approbation n° 4128 et 4150) de l’Ecole de Médecine de l’Université Shinshu, à Matsumoto, au Japon.
Déclaration de consentement éclairé
Le consentement éclairé de tous les sujets participant à l’étude a été obtenu
Conflits d’intérêts
Les auteurs ne déclarent aucun conflit d’intérêt directement lié au contenu de cette étude.
Notes de bas de page
Note de l’éditeur : le MDPI reste neutre en ce qui concerne les revendications juridictionnelles dans les cartes publiées et les affiliations institutionnelles.
Références
1. Walboomers J.M., Jacobs M.V., Manos M.M., Bosch F.X., Kummer J.A., Shah K.V., Snijders P.J., Peto J., Meijer C.J., Muñoz N. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. J. Pathol. 1999;189:12–19. doi: 10.1002/(SICI)1096-9896(199909)189:1<12::AID-PATH431>3.0.CO;2-F. [PubMed] [CrossRef] [Google Scholar]
2. FUTURE II Study Group Quadrivalent vaccine against human papillomavirus to prevent high-grade cervical lesions. N. Engl. J. Med. 2007;356:1915–1917. doi: 10.1056/NEJMoa061741. [PubMed] [CrossRef] [Google Scholar]
3. Jeurissen S., Makar A. Epidemiological and economic impact of human papillomavirus vaccines. Int. J. Gynecol. Cancer. 2009;19:761–771. doi: 10.1111/IGC.0b013e3181a130c0. [PubMed] [CrossRef] [Google Scholar]
4. The Ministry of Health, Labour and Welfare [(accessed on 8 June 2021)]; Available online: http://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou28/pdf/kankoku_h25_6_01.pdf (In Japanese)
5. Kinoshita T., Abe R., Hineno A., Tsunekawa K., Nakane S., Ikeda S. Peripheral sympathetic nerve dysfunction in adolescent Japanese girls following immunization with the human papillomavirus vaccine. Intern. Med. 2014;53:2185–2200. doi: 10.2169/internalmedicine.53.3133. [PubMed] [CrossRef] [Google Scholar]
6. Ozawa K., Hineno A., Kinoshita T., Ishihara S., Ikeda S. Suspected adverse effects after human papillomavirus vaccination: A temporal relationship between vaccine administration and the appearance of symptoms in Japan. Drug Saf. 2017;40:1219–1229. doi: 10.1007/s40264-017-0574-6. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
7. Martínez-Lavín M., Amezcua-Guerra L. Serious adverse events after HPV vaccination: A critical review of randomized trials and post-marketing case series. Clin. Rheumatol. 2017;36:2169–2178. doi: 10.1007/s10067-017-3768-5. [PubMed] [CrossRef] [Google Scholar]
8. Blitshetyn S., Brinth L., Hendrickson J.E., Martínez-Lavín M. Autonomic dysfunction and HPV immunization: An overview. Immunol. Res. 2018;66:744–754. doi: 10.1007/s12026-018-9036-1. [PubMed] [CrossRef] [Google Scholar]
9. Hirai T., Kuroiwa Y., Hayashi T., Uchiyama M., Nakamura I., Yokota S., Nakajima T., Nishioka K., Iguchi Y. Adverse effects of human papillomavirus virus vaccination on central nervous system: Neuro-endocrinological disorders of hypothalamo-pituitary axis. Auton. Nerv. Syst. 2016;53:49–64. doi: 10.1016/j.autneu.2016.09.011. [CrossRef] [Google Scholar]
10. Larson H. The world must accept that HPV vaccine is safe. Nature. 2015;528:9. doi: 10.1038/528009a. [PubMed] [CrossRef] [Google Scholar]
11. Hviid A., Svanström H., Schekker N.M., Grönlund O., Pasternak B., Arnheim-Dahlström L. Human papillomavirus vaccination of adult women and risk of autoimmune and neurological diseases. J. Intern. Med. 2017;283:154–165. doi: 10.1111/joim.12694. [PubMed] [CrossRef] [Google Scholar]
12. Phillips A., Patel C., Pillsbury A., Brotherton J., Macartney K. Safety of human papillomavirus vaccines: An updated review. Drug Saf. 2018;41:329–346. doi: 10.1007/s40264-017-0625-z. [PubMed] [CrossRef] [Google Scholar]
13. Phillips A., Hickie M., Totterdell J., Brotherton J., Dey A., Hill R., Snelling T., Macartney K. Adverse events following HPV vaccination: 11 years of surveillance in Australia. Vaccine. 2020;38:6038–6046. doi: 10.1016/j.vaccine.2020.06.039. [PubMed] [CrossRef] [Google Scholar]
14. Blitshteyn S. Postural tachycardia syndrome following human papillomavirus vaccination. Eur. J. Neurol. 2014;21:135–139. doi: 10.1111/ene.12272. [PubMed] [CrossRef] [Google Scholar]
15. Brinth L., Theibel A.C., Pors K., Mehlsen J. Suspected side effects to the quadrivalent human papillomavirus vaccine. Dan. Med. J. 2015;62:A5064. [PubMed] [Google Scholar]
16. Brinth L.S., Pors K., Theibel A.C., Mehlsen J. Orthostatic intolerance and postural tachycardia syndrome as suspected adverse effects of vaccination against human papillomavirus. Vaccine. 2015;33:2602–2605. doi: 10.1016/j.vaccine.2015.03.098. [PubMed] [CrossRef] [Google Scholar]
17. Palmieri B., Poddighe D., Vadalà M., Laurino C., Carnovale C., Clementi E. Severe somatoform and dysautonomic syndromes after HPV vaccination: Case series and review of literature. Immunol. Res. 2017;65:106–116. doi: 10.1007/s12026-016-8820-z. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
18. Martínez-Lavín M. Fibromyalgia-like illness in 2 girls after human papillomavirus vaccination. J. Clin. Rheumatol. 2014;20:392–393. doi: 10.1097/RHU.0000000000000165. [PubMed] [CrossRef] [Google Scholar]
19. Martinez P. Motor and Sensory Clinical Findings in Girls Vaccinated against the Human Papillomavirus from Carmen de Bolivar, Colombia. [(accessed on 8 June 2021)]; Available online: https://pompiliomartinez.wordpress.com/2016/03/04/motor-and-sensory-clinical-findings-in-girls-vaccinated-against-the-human-papillomavirus-from-carmen-de-bolivar-colombia/
20. Chandler R.E. Safety concerns with HPV vaccines continue to linger: Are current vaccine pharmacovigilance practices sufficient? Drug Saf. 2017;40:1167–1170. doi: 10.1007/s40264-017-0593-3. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
21. The Ministry of Health, Labour and Welfare [(accessed on 8 June 2021)]; Available online: http://www.mhlw.go.jp/file/05-Shingikai-10601000-Daijinkanboukouseikagakuka-Kouseikagakuka/0000161349.pdf (In Japanese)
22. The Ministry of Health, Labour and Welfare [(accessed on 8 June 2021)]; Available online: http://www.mhlw.go.jp/file/05-Shingikai-10601000-Daijinkanboukouseikagakuka-Kouseikagakuka/0000161329.pdf (In Japanese)
23. Matsudaira T., Takahashi Y., Matsuda K., Ikeda H., Usui K., Obi T., Inoue Y. Cognitive dysfunction and regional cerebral blood flow changes in Japanese females after human papillomavirus vaccination. Neurol. Clin. Neurosci. 2016;4:220–227. doi: 10.1111/ncn3.12083. [CrossRef] [Google Scholar]
24. Stewart J.M. Autonomic nervous system dysfunction in adolescents with postural orthostatic tachycardia syndrome and chronic fatigue syndrome is characterized by attenuated vagal baroreflex and potentiated sympathetic vasomotion. Pediatr. Res. 2000;48:218–226. doi: 10.1203/00006450-200008000-00016. [PubMed] [CrossRef] [Google Scholar]
25. Karas B., Grubb B.P., Boeth K., Kip K. The postural orthostatic tachycardia syndrome: A potentially treatable cause of chronic fatigue, exercise intolerance, and cognitive impairment in adolescents. Pacing Clin. Electrophysiol. 2000;23:344–351. doi: 10.1111/j.1540-8159.2000.tb06760.x. [PubMed] [CrossRef] [Google Scholar]
26. Halicka M., Vittersø A.D., Proulx M.J., Bultitude J.H. Neuropsychological changes in complex regional pain syndrome (CRPS) Behav. Neurol. 2020;2020:4561831. doi: 10.1155/2020/4561831. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
27. Ocon A.J. Caught in the thickness of brain fog: Exploring the cognitive symptoms of chronic fatigue syndrome. Front. Physiol. 2013;4:63. doi: 10.3389/fphys.2013.00063. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
28. Meyer C., Heidecke H. Antibodies against GPCR. Front Biosci. 2018;23:2177–2194. [PubMed] [Google Scholar]
29. Yub X., Stavrakis S., Hill M.A., Huang S., Reim S., Lin H., Khan M., Hamlett S., Cunningham M.W., Kem D.C. Autoantibody activation of beta-adrenergic and muscarinic receptors contributes to an “autoimmune” orthostatic hypotension. J. Am. Soc. Hypertens. 2012;6:40–47. doi: 10.1016/j.jash.2011.10.003. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
30. Ruzieh M., Batizy L., Dasa O., Oostra C., Grubb B. The role of autoantibodies in the syndromes of orthostatic intolerance: A systemic review. Scand. Cardiovasc. J. 2017;51:243–247. doi: 10.1080/14017431.2017.1355068. [PubMed] [CrossRef] [Google Scholar]
31. Kohr D., Singh P., Tschernatsch M., Kaps M., Pouokam E., Diener M., Kummer W., Birklein F., Vincent A., Goebel A., et al. Autoimmunity against the β2 adrenergic receptor and muscarinic-2 receptor in complex regional pain syndrome. Pain. 2011;152:2690–2700. doi: 10.1016/j.pain.2011.06.012. [PubMed] [CrossRef] [Google Scholar]
32. Dubuis E., Thompson V., Leite M.I., Blaes F., Maihofner C., Greensmith D., Vincent A., Shenker N., Kuttikat A., Leuwer M., et al. Longstanding complex regional pain syndrome is associated with activating autoantibodies against alpha-1a adrenoreceptors. Pain. 2014;155:2408–2417. doi: 10.1016/j.pain.2014.09.022. [PubMed] [CrossRef] [Google Scholar]
33. Loebel M., Grabowski P., Heidecke H., Bauer S., Hanitsch L.G., Wittke K., Meisel C., Reinke P., Volk H.D., Fluge Ø., et al. Antibodies to β adrenergic and muscarinic cholinergic receptors in patients with chronic fatigue syndrome. Brain Behav. Immun. 2016;52:32–39. doi: 10.1016/j.bbi.2015.09.013. [PubMed] [CrossRef] [Google Scholar]
34. Hendrickson J.E., Hendrickson E.T., Gehrie E.A., Sidhe D., Wallukat G., Schimke I., Tormey C.A. Complex regional pain syndrome and dysautonomia in a 14-year-old girl responsive to therapeutic plasma exchange. J. Clin. Apher. 2016;31:368–374. doi: 10.1002/jca.21407. [PubMed] [CrossRef] [Google Scholar]
35. Hendrickson J.E., Tormey C.A. Human papilloma virus vaccination and dysautonomia: Consideration for autoantibody evaluation and HLA typing. Vaccine. 2016;34:4468. doi: 10.1016/j.vaccine.2016.05.029. [PubMed] [CrossRef] [Google Scholar]
36. Blitshteyn S., Brook J. Postural tachycardia syndrome (POTS) with anti-NMDA receptor antibodies after human papillomavirus vaccination. Immunol. Res. 2017;65:282–284. doi: 10.1007/s12026-016-8855-1. [PubMed] [CrossRef] [Google Scholar]
37. Schofield J.R., Hendrickson J.E. Autoimmunity, autonomic neuropathy, and the HPV vaccination: A vulnerable subpopulation. Clin. Pediatr. 2018;57:603–606. doi: 10.1177/0009922817728701. [PubMed] [CrossRef] [Google Scholar]
38. Hineno A., Ikeda S., Scheibenbogen C., Heidecke H., Schulze-Forster K., Junker J., Riemekasten G., Dechend R., Dragun D., Shoenfeld Y. Autoantibodies against autonomic nerve receptors in adolescent Japanese girls after immunization with human papillomavirus vaccine. Ann. Arthritis Clin. Rheumatol. 2019;2:1014. [Google Scholar]
39. Simms K.T., Hanley S.J.B., Smith M.A., Keane A., Canfell K. Impact of HPV vaccine hesitancy on cervical cancer in Japan: A modelling study. Lancet Public Health. 2020;5:e223–e234. doi: 10.1016/S2468-2667(20)30010-4. [PubMed] [CrossRef] [Google Scholar]
40. Cervantes J.L., Doan A.H. Discrepancies in the evaluation of the safety of the human papillomavirus vaccine. Mem. Inst. Oswaldo Cruz. 2018;113:e180063. doi: 10.1590/0074-02760180063. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
41. Chambuso R.S., Rebello G., Kaambo E. Personalized human papillomavirus vaccination for persistence of immunity for cervical cancer prevention: A critical review with experts’ opinions. Front. Oncol. 2020;10:548. doi: 10.3389/fonc.2020.00548. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
42. Wick G. Allowing an Open Discussion of the Side Effects of Vaccines. [(accessed on 8 June 2021)]; Available online: https://science.sciencemag.org/content/allowing-open-discussion-side-effects-vaccines
Voici un témoignage bouleversant (légèrement raccourci) de 2019 :
Mon histoire de lésions causées par le vaccin HPV Gardasil
[Source : cga.ct.gov]
Par Brianne Neal
En ce qui concerne mes blessures dues à cette vaccination, l’histoire est très claire, noire et blanche : j’étais en bonne santé et me sentais bien depuis toujours, jusqu’à l’âge de 26 ans et la fin de mon diplôme d’infirmière BSN (NdT : BSN pour Bachelor of Science in Nursing – Baccalauréat en sciences infirmières) lorsque j’ai reçu la première des 3 injections Gardasil-7, et ensuite je ne l’étais plus.
J’ai consenti au vaccin Gardasil en tant que fiancée d’un militaire, il s’agissait d’un vaccin recommandé par l’armée à toutes les épouses et à tous les proches, et je voulais faire tout ce qui était « bien » et appartenir à l’armée, et être la parfaite « femme de l’armée ». Je n’avais pas réalisé que la plupart des épouses avaient refusé cette vaccination.
Je n’ai reçu aucune information sur les excipients ou les ingrédients de ce vaccin, ni sur les risques et les effets indésirables potentiels lorsque je me suis rendue chez mon médecin pour le recevoir. J’ai demandé précisément à quoi il servait – on m’a dit qu’il s’agissait de prévenir le cancer du col de l’utérus – et si j’avais des raisons de m’inquiéter ou de renoncer à la piqûre, et on m’a bien sûr répondu : « Absolument pas, nous en administrons tout le temps à des filles beaucoup plus jeunes ».
Mes symptômes de fatigue extrême et de maux de tête violents et fréquents ont été pratiquement immédiats. J’ai déménagé du Texas dans l’État de Washington avec mon mari peu de temps après la première injection de Gardasil et, dans un premier temps, j’ai mis mes symptômes sur le compte du déménagement, du changement et même du climat de l’État de Washington. Mais ils ont empiré. J’ai commencé à avoir des frissons tous les soirs sans raison, j’avais souvent des vertiges et je devais rester assise le plus possible pour éviter les étourdissements. Je n’avais guère d’appétit et je devais me forcer à manger, mais j’avais commencé à prendre du poids. Je me sentais « fatiguée » et « pas bien », et j’ai dû abandonner mon programme de transfert pour terminer mon diplôme.
Les mois appropriés s’étaient écoulés et il était temps de recevoir la deuxième dose de Gardasil-7. Je n’oublierai jamais cette belle journée de Washington et les événements fatidiques qui se sont produits. Je me suis rendue au Planning Familial pour mon deuxième vaccin de la série, car j’étais entre deux assurances maladie pendant une courte période et le vaccin était proposé à un prix raisonnable. Je me souviens que l’assistante sociale de la clinique a sorti le flacon de sa boîte et qu’elle y a apposé un grand autocollant entouré d’une épaisse ligne rouge. « Qu’est-ce que c’est que ça ? » lui ai-je demandé. Elle m’a répondu qu’elle devait m’informer que cette injection était connue pour être douloureuse et qu’il était recommandé de l’administrer à des patientes assises plutôt que debout. Je me souviens de mon hésitation et de mon malaise à ce sujet, mais encore une fois, voulant répondre aux attentes à mon égard, ayant déjà reçu la première injection et ayant appris que je devais recevoir les trois vaccins de la série pour être efficace, je me suis soumise et j’ai reçu le coup dévastateur qu’a été la deuxième injection Gardasil-7.
Le bras dans lequel j’ai reçu la piqûre a immédiatement ressenti une douleur atroce, tout le long du bras et jusqu’au bout des doigts. En silence, des larmes ont coulé de mes yeux. J’étais assis là, effrayée, et je me disais : « Ce n’est pas normal ». C’était comme si Mohamed Ali, au sommet de sa carrière, venait de frapper mon biceps d’un coup de poing, et j’étais complètement abasourdie.
La maladie qui a suivi cette deuxième piqûre a été féroce et immédiate. Ma fatigue est devenue presque narcoleptique, et mes articulations et mes muscles m’ont fait souffrir de manière insupportable, en permanence. Mes maux de tête sont devenus atroces et encore plus fréquents. J’ai rapidement développé un syndrome de tachycardie orthostatique posturale (POTS) et je m’évanouissais souvent en me levant. J’ai commencé à avoir des crises d’épilepsie, régulièrement. Mon cerveau est devenu brumeux et dispersé, et non seulement je confondais des mots que j’avais connus toute ma vie, et je me perdais à deux pâtés de maisons de chez moi, mais j’avais littéralement mal à la tête en essayant de penser. J’ai perdu 30 kilogrammes, j’ai fait un arrêt cardiaque et mon cœur a développé une arythmie sévère. Mes mains tremblaient de manière incontrôlée.
Avec l’augmentation de la fréquence de mes crises, je suis devenue une habituée de l’hôpital général local, qui ne savait plus quelle était la cause de mes maux. Mon mari m’a dit, il y a quelques années, que les ambulanciers qui venaient à la maison lorsque j’étais inconsciente après des crises étaient souvent les mêmes personnes, et qu’ils lui avaient raconté qu’à cette époque, il y avait deux autres filles dans la même zone de couverture ambulancière qui, comme moi, souffraient de ces symptômes graves, mais idiopathiques. Mes symptômes neurologiques sont devenus encore plus graves. Mon élocution a été radicalement affectée, et ce que je pouvais dire donnait l’impression que j’avais un accent étranger ou, à d’autres moments, comme si j’étais sourde. Je présentais plus d’une aphasie. J’ai perdu toute fonction motrice fine dans mes mains et je ne pouvais pas saisir des couverts ou de la nourriture pour me nourrir ou tenir un instrument d’écriture. Mon mari a enroulé à maintes reprises des serviettes autour des fourchettes et des cuillères avec plusieurs couches de ruban adhésif pour que je puisse essayer de me nourrir, et ma nourriture devait être coupée en très petits morceaux. Je trébuchais sur mes propres pieds lorsque j’étais suffisamment stable pour me tenir debout avec de l’aide, ce qui n’arrivait pas souvent. J’ai même connu des périodes où je ne contrôlais pas ma continence. Comme si toutes les choses effrayantes qui m’arrivaient n’étaient pas suffisantes, je devais maintenant être dépouillée de la dernière partie de ma dignité, sachant que je ne pouvais pas garantir que je n’urinerais pas ou pire sur moi-même, ce qui m’anéantissait. Ma disposition était si mauvaise et mes crises si constantes que je n’ai même pas remarqué que j’avais eu un AIT (accident ischémique transitoire), également connu sous le nom de « mini-AVC » pendant cette période. L’IRM de mon cerveau l’a révélé quelques mois plus tard. Ma mère a dû quitter mon père sur la côte est et venir vivre avec mon mari et moi pendant un an, car j’étais très handicapée à l’époque.
Au moment où l’IRM a été demandée, tout mon système digestif était en panne ; je ne pouvais ni manger ni boire de l’eau – mon corps en expulsait violemment le contenu. Mon mari était alors affecté au premier groupe de forces spéciales à Washington, et l’un des médecins de combat de son équipe lui a proposé d’apprendre à accrocher des poches de perfusion chez nous pour moi, et à s’administrer les perfusions lui-même. Ne pas pouvoir digérer l’eau est un état extrêmement grave et nous étions rapidement à court d’options et de ressources. J’étais à l’hôpital tous les jours à cette époque, mais les médecins n’avaient pas de réponse et se détournaient de moi.
Une autre épouse de militaire, qui était au courant de la gravité de ma maladie, nous a orientés vers une infirmière praticienne qui avait exercé la médecine allopathique pendant 45 ans et qui facilitait désormais les remèdes holistiques parallèlement aux traitements allopathiques. Elle m’a orientée vers un médecin naturopathe et, entre-temps, a amélioré mes problèmes digestifs en effectuant des tests qui ont permis de déterminer que mon corps ne produisait pas d’acide gastrique du tout et que c’était la raison pour laquelle mon corps vidait immédiatement mon estomac, parce qu’il savait que je ne pouvais pas digérer le contenu de mon estomac. Il est étonnant de constater à quel point les comprimés de chlorhydrate de bétaïne et de pepsine ont fait une énorme différence dans ma digestion, tout comme le vinaigre de cidre de pomme. J’ai pu absorber un peu de nourriture et un peu de liquide, mais j’avais encore toute une montagne à gravir pour me remettre de mes graves difficultés neurologiques. Les naturopathes avaient vu la même présentation à de nombreuses reprises, de plus en plus fréquemment au cours des dernières années. Ils ont effectué toute une série de tests sur les substances toxiques et les métaux lourds, et mes chiffres étaient hors normes. J’avais pour l’essentiel été empoisonnée, et beaucoup de ces poisons avaient atteint mon cerveau et mes tissus neuronaux.
Lorsque tout a été dit et terminé, mes nombreux diagnostics comprenaient : la thyroïdite de Hashimoto, la maladie d’Addison avec trois crises d’Addison distinctes, la fibromyalgie, le prolapsus de la valve mitrale, la polyarthrite rhumatoïde – avec une concentration dans mon bras gauche et le côté gauche de ma colonne cervicale ; le même biceps où j’ai reçu la deuxième injection de la série Gardasil 7, le syndrome de l’intestin irritable, la discopathie dégénérative, les polypes cervicaux et les ovaires kystiques – pour n’en nommer que quelques-uns. Aujourd’hui encore, la douleur intramusculaire et nerveuse dans mon bras gauche, à l’endroit où j’ai reçu la deuxième injection de Gardasil, persiste. Elle n’a jamais disparu. Mes nombreux spécialistes n’ont jamais pu mettre un nom sur mes déficits neurologiques.
Au cours des années qui ont suivi, j’ai rencontré de nombreuses femmes dont les sagas médicales étaient extrêmement similaires, des femmes d’âges différents, venant d’endroits différents, d’ethnies différentes et de milieux socio-économiques différents – la SEULE chose que nous avions toutes en commun était d’avoir reçu le vaccin Gardasil.
Grâce à de nombreuses années de désintoxication médicalement assistée, de chélation, d’alimentation biologique, de sauna, de séances de caisson hyperbare, de thérapie physique, d’ergothérapie, de thérapie psychologique, d’innombrables suppléments de haute qualité recommandés par les médecins et de médicaments allopathiques appropriés, j’ai pu retrouver ce qui étaient mes déficits neurologiques. Mes céphalées en grappe sont désormais contrôlables, mais d’autres diagnostics subsistent, chacun à des degrés divers qui varient en fonction du stress. Je suis incapable d’occuper un emploi conventionnel. Je fonctionne très bien pour mes diagnostics et j’ai de nombreuses journées décentes et productives, mais il y a encore des jours où je dois prendre du répit dans les limites sûres de ma propre maison.
J’en suis arrivée à un point où les médecins allopathes et holistiques ont dit que j’étais suffisamment en bonne santé avec les médicaments et que j’avais été bien dépistée lors des examens pré conceptionnels, et que j’avais également de bonnes réserves de vitamines, et j’ai reçu le feu vert pour commencer à essayer de concevoir un enfant. C’était il y a plus de trois ans. J’ai 34 ans et la réserve ovarienne d’une jeune femme de 19 ans, mais j’ai fait plusieurs fausses couches, y compris une fausse couche manquée au deuxième trimestre. Bien qu’il ne soit pas totalement inaccessible, il semble que mon parcours vers la maternité sera compliqué et nécessitera des thérapies et de l’aide.
J’AVAIS 26 ANS LORSQUE J’AI ÉTÉ VACCINÉE. JE N’AI JAMAIS REÇU LA TROISIÈME ET DERNIÈRE INJECTION DE LA SÉRIE GARDISIL 7. JE NE PEUX MÊME PAS IMAGINER CE QUE CELA AURAIT FAIT À MON CORPS D’ADOLESCENTE QUI N’ÉTAIT PAS ENCORE COMPLÈTEMENT DÉVELOPPÉ !!!
LE JAPON A INTERDIT CE VACCIN CAR DES DIZAINES DE JEUNES FILLES ONT ÉTÉ BLESSÉES ET PARALYSÉES LORS DE SON INTRODUCTION DANS LE PAYS.
LES MÉDECINS ALLOPATHES NE SONT PAS FORMÉS AUX EFFETS INDÉSIRABLES GRAVES ATTRIBUÉS À CETTE VACCINATION. LES SPÉCIALISTES M’ONT DIT À PLUSIEURS REPRISES QU’ILS NE SAVAIENT PAS COMMENT M’AIDER.
SI C’ÉTAIT À REFAIRE, JE NE ME SOUMETTRAIS JAMAIS, JAMAIS, À CETTE VACCINATION.
JE SUIS CHRÉTIENNE ET, AU LYCÉE, J’AI SUIVI UN COURS D’ÉDUCATION SEXUELLE APPROFONDI PORTANT SUR LES MÉTHODES DE PRÉVENTION DES MALADIES SEXUELLEMENT TRANSMISSIBLES. CES CONVICTIONS ET CES MÉTHODES ONT FONCTIONNÉ POUR MOI.
J’AI TOUJOURS EU UN COL DE L’UTÉRUS ET DES FROTTIS SAINS ET MAINTENANT JE DOIS RÉGULIÈREMENT ME FAIRE ENLEVER DES POLYPES DU COL DE L’UTÉRUS.
CE VACCIN N’A JAMAIS ÉTÉ TESTÉ POUR SES EFFETS MUTAGÈNES, CANCÉRIGÈNES OU DE DIMINUTION DE LA FERTILITÉ – OFFICIELLEMENT. CEPENDANT, LES PREUVES ANECDOTIQUES SONT ACCABLANTES ET MONTRENT QUE CE VACCIN PROVOQUE TOUS CES EFFETS NÉGATIFS.
S’IL VOUS PLAÎT, S’IL VOUS PLAÎT, ÉCOUTEZ MES APPELS DÉSESPÉRÉS !!! S’IL VOUS PLAÎT, NE SOUMETTEZ PAS VOS PRÉCIEUX ENFANTS À CE VACCIN INUTILE !!!
MON CORPS ÉTAIT DÉVELOPPÉ, FORT ET SAIN, ET MAINTENANT JE NE SERAI PLUS JAMAIS LA MÊME. JE SOUFFRIRAI DE DOULEURS CHRONIQUES SÉVÈRES JUSQU’À LA FIN DE MA VIE.
Pour les anglophones voici la notice qui accompagne le vaccin Gardasil 9 :
https://www.merck.com/product/usa/pi_circulars/g/gardasil_9/gardasil_9_pi.pdf
J’ai une question : pour quelle raison cette injection visiblement donnée pour prévenir le cancer du col de l’utérus est-elle administrée à des GARCONS ?
Les principaux rabbins de Lakewood mettent en garde contre l’utilisation du vaccin HPV Gardasil
[Source : https://www.emes.news]
L’article commence par une lettre signée au printemps 2021 par de grands rabbins de Lakewood (New Jersey), exhortant les gens à s’abstenir de recevoir le vaccin Gardasil.

La lettre de Lakewood… indique que « le vaccin a tragiquement infligé à de nombreux enfants de notre communauté des blessures graves qui ont changé leur vie ».
Cela correspond à ce que des milliers de femmes et de filles (ainsi que des garçons – boys – NdT : les images de la vidéo sont bouleversantes) du monde entier ont déclaré à propos de ce vaccin. Plusieurs documentaires ont été produits (voir ici, ici, ici et ici) qui décrivent ces expériences horribles et douloureuses ainsi que la négligence et le ridicule que ces victimes de dommages causés par les vaccins (y compris la paralysie, la ménopause chez les adolescentes et la mort) ont enduré dans leurs efforts pour obtenir une reconnaissance et une indemnisation.
(Il est difficile de trouver des informations précises à ce sujet en utilisant Google, probablement parce qu’Alphabet Inc., la société mère de Google, possède des entreprises partenaires avec des sociétés pharmaceutiques, notamment GlaxoSmithKline, Novartis, Sanofi, and Pfizer et others) (NdT : GSK pour GlaxoSmithKline, others signifie « autres »)
Il convient de noter que lors des essais cliniques du Gardasil, Merck a fait vacciner les jeunes filles du groupe de contrôle (c’est-à-dire celles qui n’ont pas reçu le vaccin) peu de temps après la fin de l’essai.
Cela a empêché la science de constater d’éventuels effets à long terme en comparant les résultats à long terme du groupe ayant reçu le vaccin à ceux du groupe n’ayant pas reçu le vaccin. Pourquoi Merck essaierait-il de détruire ce type de preuves scientifiques ? La science ne cherche-t-elle pas toujours à obtenir des résultats à long terme ?
Un schéma identique de sabotage scientifique a lieu aujourd’hui, les personnes qui faisaient partie du groupe de contrôle pour la piqûre de COVID-19 se sont ensuite vu injecter la piqûre elle-même, ce qui nous empêche de découvrir les effets indésirables à long terme de cette injection covid.
(Merck s’est également associé à Johnson & Johnson (partnered with Johnson & Johnson)pour l’injection de COVID. Johnson & Johnson a également un long passé de fraude et d’autres condamnations à son encontre). (long history of fraud and other convictions)
Il convient également de noter que Merck, le fabricant du vaccin Gardasil, est la même société qui a créé le Vioxx. Selon drugwatch , « le Vioxx était autrefois un médicament populaire pour traiter l’arthrite. Mais le fabricant Merck & Co. l’a retiré du marché en 2004 pour des raisons de sécurité. Des recherches ont établi un lien entre le médicament et des milliers de crises cardiaques mortelles ».
Même avant le retrait du Vioxx en 2004, des médecins du monde entier ont exprimé leur vive inquiétude face aux effets secondaires graves et aux décès qu’ils observaient chez leurs patients qui utilisaient le Vioxx.
Au lieu d’enquêter sur ces préoccupations et de retirer le produit du marché, Merck a décidé de passer à l’offensive. Selon The Australian, d’après des courriels internes de l’entreprise divulgués à l’époque devant les tribunaux australiens, Merck avait déclaré qu’elle attaquerait tout médecin qui remettrait en question la sécurité du Vioxx, et que « nous pourrions avoir besoin de les rechercher et de les détruire là où ils vivent », créant ainsi une liste de médecins dissidents à abattre.
Le courrier électronique, qui a été révélé au tribunal fédéral de Melbourne dans le cadre d’une action collective contre le laboratoire pharmaceutique, contenait les mots « neutraliser », « neutralisé » ou « discréditer » en regard des noms de certains médecins.
Merck est également le fabricant du vaccin ROR, utilisé pour prévenir les oreillons, la rougeole et la rubéole, et détient les droits de licence exclusifs lui permettant de vendre ce vaccin aux États-Unis.
En 2010, plusieurs scientifiques de Merck ont dénoncé le fait que la société avait délibérément menti sur l’efficacité de la partie du vaccin ROR contre les oreillons en falsifiant des données. En fait, ils ont affirmé que le vaccin contre les oreillons ne fonctionnait pas vraiment, sur la base de données véridiques.
À la suite de cette découverte, le gouvernement des États-Unis a lui-même porté plainte contre Merck. Ce procès est connu sous le nom de United States versus Merck. Ce procès dure depuis plus de dix ans. Il y a environ un an, les dossiers de l’affaire ont été mis sous scellés.
L’auteur se demande pourquoi il serait nécessaire de dissimuler les dossiers dans le cas où Merck serait réellement innocent de ces allégations. Ne souhaiteraient-ils pas que les dossiers ne soient pas scellés, afin que leur dossier puisse être justifié devant le tribunal de l’opinion publique ?
Nous avons pu obtenir des copies de la plainte originale déposée par le gouvernement : Download as PDF (NdT : voilà un document qui mériterait d’être traduit)
Tout ce qui précède a permis de documenter les dommages causés par le vaccin contre le papillomavirus, mais ce dernier est-il au moins efficace dans son objectif déclaré de prévention du cancer du col de l’utérus ?
Il semble évident que le vaccin HPV est une vaste escroquerie, comme tant d’autres, et que les souffrances humaines qu’il provoque ne servent à rien d’autre qu’à remplir les poches de ceux qui le fabriquent et le distribuent.
J’ai demandé à mes lecteurs de m’aider à trouver des informations à ce sujet.
Un abonné, docteur en médecine, m’a envoyé deux courriels que je reproduis ici sous forme abrégée. Toute documentation supplémentaire que d’autres lecteurs pourraient m’envoyer à l’adresse truth613@substack.com, ou dans les commentaires, serait très appréciée.
Gardasil était une fraude dès le premier jour. Comme mon camarade de classe du programme de doctorat en médecine de l’université de New York a passé six ans à étudier le papillome (virus de la verrue), je n’ai pas pu m’empêcher d’apprendre tout ce qu’il y avait à savoir à ce sujet. Ce virus est bien connu et intensément étudié depuis un siècle maintenant. Certains l’ont toujours soupçonné de provoquer le cancer, mais après cent ans, il n’y a toujours pas la moindre preuve crédible qu’il provoque autre chose que des verrues.
Lorsque le Gardasil a été mis sur le marché, il était censé « réduire le cancer du col de l’utérus de 75 % » (chiffre approximatif, mais ENORME). J’ai tout de suite senti le pot aux roses, mais comment pouvais-je dire à mes patientes de refuser un « vaccin » qui entraînait une réduction aussi spectaculaire du nombre de cancers ? Je n’ai donc rien dit.
Mais le battage médiatique s’est poursuivi, et il est devenu évident qu’ils allaient administrer ce vaccin à des petites écolières.
Finalement, la puanteur de la fraude est devenue trop accablante et j’ai pris le temps de faire des recherches. La première chose que j’ai lue était la notice, qui indiquait avec précision que le « vaccin » était destiné à lutter contre le papillomavirus, et non contre le « cancer du col de l’utérus ». La notice ne prétendait pas être un remède contre le cancer, mais indiquait que le vaccin était conçu pour prévenir les verrues, qui « pourraient » subir une transformation maligne. Vraiment ? Comment se fait-il alors que cent ans de recherche n’aient pas permis de mettre en évidence une telle transformation maligne ? Que manque-t-il à cette image ?
J’ai ensuite recherché l’histoire de ce soi-disant « vaccin ». Les deux femmes qui ont mis au point le vaccin de Merck (je n’arrive pas à me souvenir de leurs noms maintenant), lorsqu’elles ont pris conscience des mensonges que Merck employait pour faire croire aux gens qu’il s’agissait d’un « vaccin contre le cancer », ont dénoncé publiquement la campagne de marketing de Merck. Ils sont donc en bonne compagnie avec Kary Mullis, le lauréat du prix Nobel inventeur de la PCR, et Robert Malone, l’inventeur du vaccin à ARNm.
(N’oublions pas non plus l’aide apportée par Merck dans la mise au point du gaz toxique pour les chambres à gaz d’Hitler).
Le 2ème courriel du médecin :
J’ai fait quelques recherches pour savoir ce que l’on prétend aujourd’hui à propos du HPV. À ma grande horreur, ils ont conclu que le HPV est à l’origine de « la plupart des cas » de cancer du col de l’utérus.
Est-ce que j’y crois ? Je n’y crois pas du tout. Si, après un siècle de recherche, aucun lien clair n’a pu être établi entre le HPV et le cancer, qu’est-ce qui a changé ?
Au cours des 10 à 20 dernières années, un certain nombre d’« études » ont été publiées, proclamant que la majorité des carcinomes du col de l’utérus « ont de l’ADN de papillomavirus dans leurs cellules ». Cela ne prouve pas nécessairement quelque chose, mais la première question à se poser est : « Comment cela a-t-il été déterminé ? »
La plupart des articles que j’ai essayé de consulter sont payants, et je ne paierai pas (il y a très peu de cas où j’ai appris quelque chose de valable à partir d’un article dont la lecture exigeait un paiement). Les études visibles ne font que renvoyer à des études antérieures qui posent plus de questions qu’elles n’apportent de réponses. Tout d’abord, la plupart des statistiques proviennent de pays étrangers, où la « recherche scientifique » » se traduit souvent par « « acceptation d’un pot-de-vin du gouvernement » (ou d’une entreprise pharmaceutique). Deuxièmement, qu’appelle-t-on exactement « cancer » ? Cette question est loin d’être anodine.
Tout d’abord, la théorie selon laquelle le célèbre « frottis » permet d’identifier les « lésions précancéreuses du col de l’utérus » n’a jamais été testée. J’ai demandé un jour à un pathologiste de me donner la référence d’une étude prospective randomisée comparant le taux de mortalité par cancer chez les femmes qui subissent l’inutile frottis de Papanicolaou et chez celles qui le refusent. Il m’a répondu : « Ce n’est pas possible, ce n’est pas éthique« .
« Pas éthique » ? Si l’efficacité du frottis en matière de prévention du cancer n’a jamais été testée, parce qu’un tel test ne serait pas « éthique », comment le frottis a-t-il pu atteindre le statut quasi obligatoire qui est le sien (je pense que vous connaissez la réponse à cette question : le marketing de masse et les profits des médecins et des pharmaciens).
Question suivante : Quelles sont ces lésions que l’on appelle « cancer » du col de l’utérus ? Existe-t-il des preuves qu’elles sont réellement malignes ? Ou s’agit-il simplement d’une nouvelle escroquerie au « carcinome basocellulaire » ? (Le carcinome basocellulaire, véritable vache à lait pour les dermatologues, n’est absolument pas malin, mais s’ils disaient la vérité et cessaient de l’appeler « carcinome », l’industrie dermatologique perdrait des tonnes d’argent).
En voici d’autres – merci au lecteur pour sa contribution !
La vaccination contre le HPV permet-elle de prévenir le cancer du col de l’utérus ?
[Source : journals.sagepub.com]
Claire P Rees https://orcid.org/0000-0001-5649-7835, Petra Brhlikova, et Allyson M Pollock allyson.pollock@ncl.ac.uk View all authors and affiliations (Voir tous les auteurs et leurs affiliations). Volume 113, 2ème édition – 1ère publication le 21 janvier 2020
Résumé
Nous avons procédé à une évaluation critique des essais d’efficacité de phase 2 et 3 publiés dans le cadre de la prévention du cancer du col de l’utérus chez les femmes. Notre analyse montre que les essais eux-mêmes ont généré des incertitudes significatives qui sapent les affirmations d’efficacité de ces données. Douze essais contrôlés randomisés (ECR) ont été menés sur Cervarix et Gardasil. Les populations des essais ne reflétaient pas les groupes cibles de la vaccination en raison des différences d’âge et des critères d’inclusion restrictifs des essais. L’utilisation de résultats composites et de résultats de substitution éloignés ne permet pas de déterminer les effets sur les résultats cliniquement significatifs. On ne sait toujours pas si la vaccination contre le virus du papillome humain (HPV) prévient le cancer du col de l’utérus, car les essais n’ont pas été conçus pour détecter ce résultat, qui met des dizaines d’années à se développer. Bien qu’il existe des preuves que la vaccination prévient la néoplasie intraépithéliale cervicale de grade 1 (CIN1), il ne s’agit pas d’un résultat cliniquement important (aucun traitement n’est administré). Les essais ont utilisé des résultats de substitution composites incluant la CIN1. Une efficacité élevée contre les CIN1+ (CIN1, 2, 3 et adénocarcinome in situ (AIS)) ne signifie pas nécessairement une efficacité élevée contre les CIN3+ (CIN3 et AIS), qui surviennent beaucoup moins fréquemment. Les données sont trop peu nombreuses pour que l’on puisse conclure clairement que le vaccin anti-HPV prévient les CIN3+. Il est probable que les CIN en général aient été surdiagnostiquées dans les essais, car la cytologie cervicale a été effectuée à des intervalles de 6 à 12 mois plutôt qu’à l’intervalle normal de dépistage de 36 mois. Cela signifie que les essais peuvent avoir surestimé l’efficacité du vaccin, car certaines lésions auraient régressé spontanément. De nombreux essais ont diagnostiqué une infection persistante sur la base de tests fréquents à intervalles courts, c’est-à-dire moins de six mois. Il n’est pas certain que les infections détectées disparaissent ou persistent et entraînent des modifications du col de l’utérus.
Le programme de vaccination contre le papillomavirus humain (HPV) vise à prévenir le cancer du col de l’utérus. Dans le monde, le cancer du col de l’utérus est diagnostiqué chaque année chez environ 13,1/100 000 femmes2. En règle générale, la vaccination est proposée aux jeunes filles âgées de 9 à 13 ans avant leur entrée dans la vie sexuelle et n’ayant jamais été infectées par le VPH.
Octroi des licences
– Les vaccins Gardasil, Gardasil-9 et Cervarix ont été approuvés pour la commercialisation et utilisés chez les femmes et les hommes à partir de l’âge de 9 ans dans le monde entier pour prévenir le cancer du col de l’utérus.
– L’Agence européenne des médicaments (EMA) et la Food and Drug Administration (FDA) des États-Unis ont autorisé la mise sur le marché de Gardasil en 2006, et de Cervarix en 2007 et 2009, respectivement.
– Le Gardasil-9 a été approuvé en 2014 par la FDA et en 2015 par l’EMA, mais il n’est pas encore utilisé au Royaume-Uni.
– L’EMA a homologué les trois vaccins pour les femmes et les hommes, sans limite d’âge. La FDA (NdT : Food and Drug Administration – organisme fédéral américain qui délivre les autorisations de mise sur le marché pour les médicaments et les denrées alimentaires) a autorisé Gardasil jusqu’à 26 ans et Gardasil-9 jusqu’à 45 ans pour les femmes et les hommes, et Cervarix jusqu’à 25 ans pour les femmes uniquement.
Lignes directrices
– Les centres américains de contrôle et de prévention des maladies recommandent une vaccination systématique à l’âge de 11 ou 12 ans. (La vaccination peut commencer à l’âge de 9 ans.) L’Advisory Committee on Immunization Practices (Comité Consultatif sur les Pratiques de Vaccination) recommande également la vaccination pour les femmes âgées de 13 à 26 ans qui n’ont pas été suffisamment vaccinées auparavant3.
– Le Royaume-Uni utilise le Gardasil. Public Health England (NdT : Santé Publique Angleterre) conseille aux jeunes filles de se faire vacciner entre 12 et 18 ans. Immunisation Scotland propose le vaccin aux filles âgées de 11 à 13 ans. Il est prévu d’étendre le vaccin aux garçons âgés de 12 à 13 ans en Angleterre et en Écosse.
Directives
– Les Centres américains de contrôle et de prévention des maladies recommandent « une vaccination systématique à l’âge de 11 ou 12 ans (la vaccination peut commencer à l’âge de 9 ans). L’Advisory Committee on Immunization Practices recommande également la vaccination pour les femmes âgées de 13 à 26 ans qui n’ont pas été suffisamment vaccinées auparavant » 3.
– Le Royaume-Uni utilise le Gardasil. Public Health England conseille aux jeunes filles de se faire vacciner entre 12 et 18 ans. Immunisation Scotland propose le vaccin aux filles âgées de 11 à 13 ans. Il est prévu d’étendre le vaccin aux garçons âgés de 12 à 13 ans en Angleterre et en Écosse.
Les agences de santé publique défendent la position selon laquelle il a été démontré que le vaccin prévient le cancer du col de l’utérus (voir supplément 1). Toutes ne soulignent pas systématiquement les limites des preuves ou les incertitudes dont nous allons parler.
Contexte
La complexité de l’épidémiologie des sous-types de HPV et des lésions utilisées comme critères de substitution pour le cancer du col de l’utérus constitue un problème majeur pour la conception des essais et des études d’efficacité, chacun ayant sa propre histoire naturelle, sa prévalence, son incidence et la force de son association avec le cancer. Ces mesures, en particulier lorsqu’elles sont combinées en tant que critères de substitution composites dans les essais, génèrent de nouvelles incertitudes.
I Infection par le HPV
Il existe plus de 100 types de HPV : 12 d’entre eux sont cancérigènes pour l’homme, selon l’Association internationale de recherche sur le cancer (IARC)4. Les types varient en prévalence, tout comme leur association avec le cancer du col de l’utérus. Les vaccins anti-HPV sont homologués contre les types oncogènes 16 et 18 et maintenant 31, 33, 45, 52 et 58 dans le Gardasil-9. Gardasil et Gardasil-9 sont également homologués contre les types 6 et 11 non oncogènes associés aux verrues génitales.
Le risque d’infection à HPV au cours de la vie est de 79 %5 ; la majorité des infections à HPV sont transitoires et 67 % disparaissent en l’espace d’un an 6. Environ 10 % des femmes sans CIN sont infectées par HPV à un moment donné 7.7 Le mécanisme de progression de l’infection à HPV vers le cancer du col de l’utérus et ses précurseurs n’est pas bien compris 4,8–11.
II Cancer du col de l’utérus et lésions précancéreuses comme critères de substitution
Les taux estimés de régression et de progression pour les CIN1, 2 et 3 sont présentés dans la Figure 1.12 Toutefois, des incertitudes subsistent en raison de problèmes méthodologiques dans les études épidémiologiques à l’origine de ces résultats12.
Figure 1 : Histoire naturelle des CNI (Données Ostör, 1993)
Infection persistante
| Taux de régression vers un col normal |  | Taux d’évolution vers le cancer du col de l’utérus |
L’IARC a reconnu que les critères d’évaluation composites dans les études d’intervention portant sur la CIN2 sont sous-optimaux13 car la CIN2 est souvent mal classée en raison de la faible reproductibilité et validité de son diagnostic14 . Les femmes présentant une CIN2 se voient actuellement proposer un traitement, ce qui complique la recherche sur l’évolution vers la CIN3.
Les femmes atteintes d’une CIN2 se voient actuellement proposer un traitement, ce qui complique les recherches sur l’évolution vers une CIN3. Une CIN3 peut se développer suite à l’évolution d’une CIN1 et d’une CIN2 ou directement suite à une infection par le HPV. Le taux de progression d’une CIN3 vers un cancer invasif est probablement plus élevé que l’estimation d’Ostör, qui est de >12 %12 . Le risque à vie peut atteindre 40 % en l’absence de dépistage et de traitement du cancer du col de l’utérus15.
Objectif
Décrire les incertitudes générées par la conception des essais d’efficacité de phase 2 et 3 pour la prévention du cancer du col de l’utérus et de ses précurseurs et la façon dont elles affectent l’interprétation des données d’efficacité.
Méthodes et analyses
Nous avons recherché dans Embase et Medline des articles relatifs à des essais contrôlés en aveugle de la vaccination contre le HPV chez les femmes, en considérant l’efficacité contre le cancer du col de l’utérus et ses précurseurs. La stratégie de recherche est décrite dans le supplément 2. Aucun essai n’a testé les vaccins Gardasil et Cervarix face à face en utilisant des résultats cliniques (plutôt que des résultats immunologiques). Nous avons examiné 35 articles publiés portant sur 12 essais de phase 2 et 3, randomisés et en aveugle, contrôlés par des vaccins non-HPV, de Gardasil et Cervarix menés entre 2001 et 2016 et évaluant l’efficacité contre le cancer du col de l’utérus et ses précurseurs (Table 1 et Figure 2) (tableau 1 et figure 2). Tout au long de cet article, nous nous référons aux essais par le nom de leur protocole, tel qu’il apparaît en gras dans la Table 1. Cependant, pour les essais 104798 et 107638, nous utilisons le nom de leurs premiers auteurs, Konno et Zhu, respectivement.
Ci-dessous : Trials (Essais)
The study was sponsored and funded by NCI but it was done under an FDA investigational new drug application (IND) for which the manufacturer has to function as sponsor (Cette étude a été parrainée et financée par le NCI, mais elle a été réalisée dans le cadre d’une demande de nouveau médicament expérimental (IND) de la FDA pour laquelle le fabricant doit faire office de promoteur doit agir en tant que sponsor.)

Figure 2. Essais contrôlés randomisés de phase 2 et 3 sur l’efficacité de la vaccination HPV.
Tableau 1. Tous les essais de phase 2 et 3 par vaccin et contrôle, promoteur, pays, dates de début et de fin, nombre et âge des participants et durée du suivi. (NdT : Voir le tableau en cliquant sur le lien https://journals.sagepub.com/doi/10.1177/0141076819899308 ).
Messages clés :
– Nous ne savons pas dans quelle mesure la vaccination contre le papillomavirus protège contre le cancer du col de l’utérus. Les essais ne se sont pas concentrés sur l’issue du cancer du col de l’utérus parce qu’ils comptaient trop peu de participantes et ne les ont pas suivies suffisamment longtemps : le cancer du col de l’utérus peut mettre des décennies à se développer.
– Les chiffres publiés à partir d’essais contrôlés randomisés peuvent surestimer l’efficacité pour les raisons suivantes : (a) les tests ont été trop fréquents dans les essais alors que, dans le monde réel, les lésions peuvent régresser spontanément ; (b) les essais ont utilisé des résultats de substitution composites, dont certains, tels que l’infection par le HPV et la CIN1, surviennent plus fréquemment que d’autres et sont très peu susceptibles d’évoluer vers un cancer ; et (c) les sous-groupes ont été analysés de manière trop approfondie.
– Les populations des essais ont une pertinence et une validité limitées pour le monde réel : par exemple, les femmes participant aux essais étaient plus âgées que la population cible ; nous ne disposons pas de suffisamment de données sur les avantages pour les femmes qui peuvent avoir été exposées au HPV avant d’être vaccinées et qui ne connaissent pas leur statut en matière de HPV.
– Nous ne disposons pas de suffisamment de données sur l’impact du vaccin sur les CIN3, qui sont plus susceptibles que les CIN1 et 2 d’évoluer vers un cancer du col de l’utérus. Nous disposons également de moins de données sur l’impact des maladies du col de l’utérus dues à n’importe quel type de HPV, plutôt que sur les seules lésions dues aux HPV 16 et 18.
– Les femmes doivent continuer à se soumettre à un dépistage régulier du cancer du col de l’utérus, car l’efficacité de la prévention des précurseurs du cancer du col de l’utérus est inférieure à 100 % et il existe davantage de types oncogènes que ceux couverts par les vaccins. Il est prouvé que le dépistage du cancer du col de l’utérus réduit de manière significative le risque de cancer du col de l’utérus chez les femmes, qu’elles aient été vaccinées ou non. Le nombre de nouveaux cancers et de décès a nettement diminué, de sorte que le cancer du col de l’utérus ne représente plus que 1 % des décès par cancer chez les femmes au Royaume-Uni (854 décès en 2016) 1.
– Les informations tirées des essais peuvent nous renseigner sur ce qui se passe entre cinq et neuf ans après la vaccination, mais nous ne savons pas si la protection diminue après cette période.
– Une étude d’observation récente fournit des preuves de l’efficacité de la vaccination contre les CIN3+ chez les filles vaccinées avant leur entrée dans la vie sexuelle. Les études d’observation en cours peuvent nous renseigner sur l’effet à long terme sur les taux de cancer du col de l’utérus, mais il faudra de nombreuses années avant que nous disposions de ces données.
Nous avons exclu les essais portant sur le vaccin monovalent contre le HPV 16 (car il n’était pas homologué et les données suggèrent que sa pharmacodynamique est différente de celle du Gardasil et du Cervarix 16 ) et l’unique essai d’efficacité du Gardasil-9 (car le contrôle était le Gardasil, et non un placebo) 17 ; ce qui, en soi, a suscité des inquiétudes 11. Nous avons choisi de nous concentrer sur les essais contrôlés randomisés, car ils offrent le niveau de preuve le plus élevé, et ce sont eux qui sont utilisés pour les décisions des organismes de réglementation et les décisions relatives au lancement des programmes de vaccination.
Nous avons également trouvé 39 méta-analyses et revues systématiques sur l’efficacité des vaccins anti-HPV, dont beaucoup se limitent à des analyses a posteriori de sous-groupes et combinent de manière inappropriée des essais dans la même analyse, par exemple pour des vaccins différents (voir complément 3). La revue Cochrane de 2018 18 a été critiquée pour ne pas avoir inclus tous les essais pertinents, pour avoir ignoré les preuves des effets néfastes et pour avoir utilisé des critères d’évaluation composites avec des histoires naturelles différentes 19.
Nous avons comparé les critères d’éligibilité, les méthodes de dépistage du HPV et des lésions cervicales, les mesures des résultats, la durée du suivi, le groupe cible et les définitions des sous-groupes utilisés dans les différents essais. Nous nous sommes concentrés sur les preuves d’efficacité pour les CIN3+ et l’infection persistante à 12 mois, qui sont considérées comme les mesures de résultats les plus strictes.
Le vaccin contre le papillomavirus prévient-il le cancer du col de l’utérus ?
Aucun des essais n’a été conçu pour déterminer l’efficacité contre le cancer du col de l’utérus. Aucun essai n’a fait état de cas de cancer du col de l’utérus ; un cas de carcinome vulvaire a été signalé dans le groupe vacciné de l’essai FUTURE I 48.
Le délai entre la première exposition au HPV et l’apparition du pic de CIN3 est de 7 à 10 ans 13 . D’après les études d’histoire naturelle, il faut encore une dizaine d’années pour que le cancer du col de l’utérus se développe 13. Tous les essais ont eu une durée moyenne de suivi de six ans ou moins, à l’exception de l’extension HPV-023 qui a eu une durée moyenne de suivi de 8,9 ans.
Le vaccin contre le HPV prévient-il les lésions précancéreuses ?
Les essais ont utilisé huit critères d’évaluation de la maladie du col de l’utérus, qui étaient tous des critères de substitution ou des critères de substitution composites (Table 2). Les résultats de substitution sont des biomarqueurs utilisés comme substituts des résultats cliniques et utilisés pour prédire les bénéfices d’une intervention. Les principaux essais préalables à la mise sur le marché ont évalué l’effet des vaccins anti-HPV sur les lésions précancéreuses, critères acceptés par les autorités comme substituts du cancer du col de l’utérus. Les résultats de substitution présentent des limites en général 54 , ainsi que pour le HPV et le cancer du col de l’utérus. L’utilisation de résultats de substitution composites (combinant deux ou plusieurs résultats de substitution) est problématique en raison des différences dans l’épidémiologie, l’histoire naturelle et la prise en charge – voir la section « Contexte » et la Figure 1 . Cinq des 12 essais (VIVIANE, V01-007, FUTURE III, V501-027, V501-041) avaient la puissance nécessaire pour obtenir des résultats composites combinant la maladie cervicale et l’infection persistante par le VPH 43,47,51–53. Quatre essais ont combiné la maladie cervicale et les verrues génitales dans le même résultat primaire (FUTURE III, V501-007 et V501-027, V501-041), ce qui a gonflé les mesures d’efficacité 47,51–53.
Tableau 2. Critères d’évaluation validés pour l’ensemble des essais.
| Critère d’évaluation alimenté | Nombre d’essais utilisant le critère d’évaluation | Vaccin utilisant le critère d’évaluation |
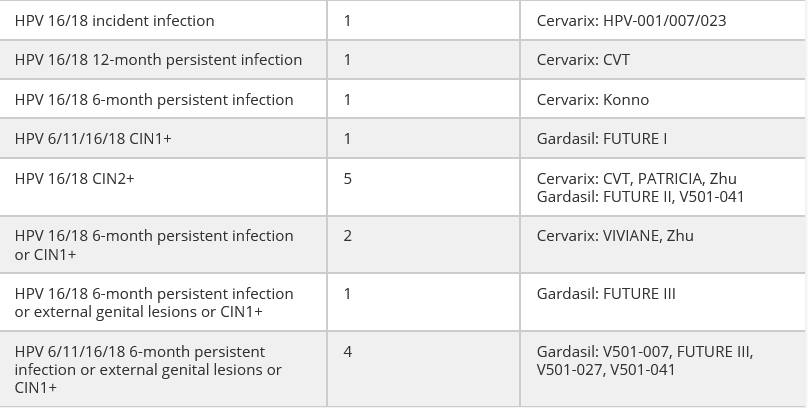
CIN 1+
Les résultats de l’essai comprenaient les critères de substitution CIN1 et CIN2, qui sont plus fréquents que les CIN3/AIS et le cancer du col de l’utérus, mais qui régressent souvent et ne posent qu’un problème clinique limité (voir la section « Contexte » et la Figure 1 ). Par exemple, l’intervention n’est pas recommandée pour les CIN1. Sept essais (FUTURE I, VIVIANE, V01-007, FUTURE III, V501-027, Zhu, V501-041) ont inclu la CIN1 avec la CIN2, la CIN3 et l’AIS dans le même résultat primaire (ce qui constitue un résultat composite), ce qui risque de gonfler l’efficacité du vaccin car il y a beaucoup plus de cas de CIN1 que de CIN2+ 43,45,47,48,51–53 .
CIN 2+
L’incidence (taux de détection) des CIN2, CIN3 et AIS dans les essais était faible, de sorte que même si de nombreux essais ont montré une grande efficacité du vaccin, c’était dans le contexte d’un très petit nombre de cas de CIN2+. Par exemple, l’essai HPV-023 a montré une grande efficacité du vaccin (100 % contre les CIN2 et CIN3 sur un suivi de neuf ans) avec une très faible incidence (seulement trois cas, tous dans le groupe témoin, sur 212 participantes)25. Les essais étaient alimentés par le nombre minimum d’événements nécessaires pour obtenir un résultat statistiquement significatif, et de nombreux essais ont été conçus pour s’arrêter une fois ce nombre atteint. Les essais étaient alimentés par le nombre minimum d’événements nécessaires pour obtenir un résultat statistiquement significatif, et de nombreux essais étaient conçus pour s’arrêter une fois ce nombre atteint. Au lieu de mener plusieurs essais de courte durée, il aurait été possible de surmonter ce problème de puissance en menant un grand essai de plus longue durée dans chaque pays.
CIN 3+
Il est généralement admis que la CIN3 est le meilleur marqueur du risque de cancer du col de l’utérus, avec des taux de progression d’au moins 12 %12. De nouvelles données suggèrent qu’il est préférable de réserver l’intervention clinique après la détection lors du dépistage aux femmes présentant une CIN355. Seuls trois des 12 essais (FUTURE I, FUTURE II, PATRICIA) ont fait état de CIN3+ ou d’AIS dans des sous-groupes représentatifs de la population cible de femmes naïves vis-à-vis du HPV (voir supplément 4)30,49,56. L’incidence des AIS dans les essais est très faible et seuls trois essais (FUTURE I, FUTURE II, PATRICIA) ont publié des résultats pour les AIS uniquement30,49,56.
Dans ces trois essais, l’efficacité du vaccin contre les CIN3 et les AIS dus aux HPV 16/18 était de 100 % (voir Supplément 4), mais les chiffres étaient faibles et les intervalles de confiance larges, parfois non significatifs (lorsque l’intervalle de confiance passe par zéro)49,56. L’efficacité du vaccin contre les CIN3 et les AIS dus à n’importe quel type de HPV variait considérablement d’un vaccin à l’autre30,56.
Quelles sont les preuves que la vaccination prévient les infections à HPV cliniquement significatives ?
Il est possible de diagnostiquer les nouvelles infections à HPV (incidentes) et les infections en cours (persistantes). Des études ont montré que la durée médiane de l’infection par le HPV 16 était de 8,5 à 19,4 mois et celle de l’infection par le HPV 18 de 7,8 à 12 mois 13.
L’essai HPV001/007/023 a utilisé l’infection incidente à HPV 16/18 comme résultat primaire20,22,25. Les résultats ne sont pas pertinents pour la prise de décision politique car le consensus actuel rapporté par l’OMS est que l’infection incidente à HPV n’est pas un résultat de substitution adéquat car elle évolue rarement vers une maladie du col de l’utérus57.
Il n’y a pas d’accord sur la période qui définit une infection persistante13 et les essais peuvent avoir surestimé l’efficacité du vaccin en choisissant des périodes plus courtes que la durée de la plupart des infections autolimitées, par exemple six mois. Dans certains essais, l’intervalle de test pour diagnostiquer une infection persistante à six mois était de quatre mois 36,47,52 ou de cinq mois44,51,53.
Un seul essai Gardasil, V501-041, a utilisé l’infection persistante à 12 mois comme critère de jugement ; cependant, les auteurs de l’étude n’ont présenté des données que pour les HPV combinés 6/11/16/18, et non pour 16/18 ou tout autre type oncogène 53 . Dans les essais sur Cervarix, l’efficacité du vaccin contre l’infection persistante à 12 mois causée par le VPH 16/18 variait de 85,3 à 100 % (voir le supplément 5) 25,27,29,33,45. L’efficacité du vaccin contre l’infection persistante à 12 mois causée par tout type de VPH oncogène variait de 10,4 % à 50,1 % dans tous les essais, avec de larges intervalles de confiance pour la plupart des essais25,27,29,33,45. Les résultats n’étaient pas statistiquement significatifs pour l’essai HPV-023 et Zhu (voir le supplément 5) 25,45.
Tous les essais n’ont pas analysé séparément les types 16 et 18 du HPV. L’incidence de l’infection par le VPH varie selon le type de VPH30. Le VPH 18 était beaucoup moins courant que le VPH 16. En combinant leurs résultats, l’efficacité contre le VPH 18 semble plus solide. Dans certains essais, les résultats concernant le HPV 18 n’étaient pas statistiquement significatifs en soi et ne l’étaient que lorsqu’ils étaient combinés aux résultats concernant le HPV 16. Par exemple, dans le sous-groupe de population per-protocole de l’essai V501-027, l’efficacité du vaccin contre l’infection persistante ou la maladie génitale à six mois (le résultat principal de l’essai) était de 100 % (59,7,100) pour le HPV 16, de 86,0 % (-8,9, 99,7) pour le HPV 18 et de 94,5 % (65,2, 99.9) pour le HPV 16/1852. Dans le sous-groupe de la cohorte conforme au protocole pour l’efficacité (ATP-E) de l’essai PATRICIA, l’efficacité du vaccin contre les CIN3+ était de 90,2 % (59,7, 98,9) pour le VPH 16, de 100 % (-8,2, 100) pour le VPH 18 et de 91,7 % (66,6, 99,1) pour le VPH 16/18, respectivement30 . Cela signifie que le vaccin pourrait ne pas protéger aussi bien contre le cancer du col de l’utérus lié au HPV 18. La proportion de cancers du col de l’utérus liés au HPV 18 varie de 13% en Amérique du Sud/Centrale à 22% en Amérique du Nord58.
Quelles sont les informations disponibles sur les résultats à long terme et sur la durée de la protection ?
Tous les essais ont duré six ans ou moins, à l’exception de l’étude de prolongation HPV-023 avec un suivi moyen de 8,9 ans (qui a maintenu l’insu et conservé un groupe témoin), qui n’a inclus que 437 des 1113 participantes initiales à HPV-00125. L’étude la plus longue sur Gardasil a été V501-041, qui a été prolongée de 30 à 78 mois avec 2601 participantes sur les 3006 initiales53.
Les caractéristiques des essais peuvent fausser les résultats en surestimant l’efficacité à long terme. Par exemple, les CIN3 liées au HPV 16/18 se présentent plus tôt que les CIN3 de type non-vaccinal, de sorte que les essais d’efficacité plus courts seront biaisés en faveur de la découverte de CIN3 liées au HPV 16/1859.
Bien que l’incidence et la progression de la maladie diffèrent dans le temps et selon l’âge, l’essai V501-007 a combiné les résultats des participantes de l’essai initial avec ceux des participantes qui ont complété une extension supplémentaire de deux ans47. Dans les essais HPV-007 et HPV-023, les résultats des participantes des essais précédents ont été pris en compte ensemble22,25.
Dans quelle mesure les femmes participant aux essais étaient-elles semblables aux groupes cibles de la vaccination ?
Les femmes participant aux essais sont généralement plus âgées que celles qui participent aux programmes de vaccination en situation réelle, et il n’est pas certain que les résultats soient similaires. Nous ne connaissons pas les taux d’efficacité chez les filles âgées de 9 à 13 ans.
Les participantes les plus jeunes aux essais étaient âgées de 15 ans et les essais n’ont pas limité le recrutement aux filles avant leur entrée dans la vie sexuelle. Il est donc probable que certaines filles aient déjà été exposées au VPH. Des sous-groupes per-protocole comptant beaucoup moins de participantes ont été utilisés pour analyser celles dont l’exposition antérieure au HPV n’était pas prouvée, mais comme indiqué précédemment, la plupart des essais n’ont pas présenté de données sur les résultats concernant les CIN3+ dans ces sous-groupes.
L’efficacité chez les filles âgées de 9 à 13 ans a été estimée à l’aide d’essais de pontage immunitaire (où les niveaux de réponse immunitaire sont mesurés) (NdT : Les études de pontage immunitaire sont des essais contrôlés, utilisant des placebos ou d’autres contrôles et des corrélats de protection tels que les paramètres immunitaires humoraux et/ou cellulaires pour établir si une intervention est efficace) plutôt qu’à l’aide de résultats cliniques60. Nous ne savons pas quel niveau de titres d’anticorps définit un niveau de substitution de protection contre le cancer du col de l’utérus ou ses précurseurs et combien de temps la protection durera (les titres anti-HPV 18 de Gardasil ne sont pas différents de l’infection naturelle dès 24 mois après la vaccination) 60. Par conséquent, il est possible que la protection s’estompe au moment du pic d’exposition lorsque la vaccination est effectuée à un âge plus précoce.
Trois essais ont recruté des femmes plus âgées (FUTURE III (24-45 ans), VIVIANE (26+) et V501-041 (20-45 ans) 42,50,53. Dans l’essai VIVIANE, un sous-ensemble allant jusqu’à 15 % de femmes ayant des antécédents d’infection ou de maladie associée au VPH a été inclus (défini par au moins deux frottis anormaux consécutifs, une colposcopie anormale ou une biopsie ou un traitement du col de l’utérus après un frottis ou une colposcopie anormaux), mais cela signifie que la cohorte totale du vaccin ne reflète peut-être pas la proportion de femmes ayant des antécédents de maladie associée au VPH dans l’ensemble de la population 42. Des restrictions fondées sur l’ADN du VPH et le statut sérologique ont ensuite été imposées pour l’inclusion dans la cohorte conforme au protocole pour l’efficacité et dans la cohorte vaccinale totale pour les sous-groupes d’efficacité. Dans FUTURE III, les femmes ayant des antécédents de verrues génitales ou de maladie du col de l’utérus, passés ou présents, ont été exclues ; les principaux tests d’efficacité ont été effectués dans le cadre des analyses d’efficacité per-protocole (EPP) spécifiques au type de VPH, qui exigeaient que les femmes soient séronégatives pour le type concerné au jour 1 et que la PCR soit négative pour ce type dans les écouvillons du col de l’utérus ou les échantillons de biopsie, ou les deux, du jour 1 jusqu’au mois 7 50. L’étude V501-041 excluait les femmes ayant eu plus de quatre partenaires sexuels et celles ayant des antécédents de verrues génitales ou de « maladie cervicale significative » – les auteurs de l’étude n’ont pas précisé ce que cela signifiait 53.
Sept essais ont exclu les femmes ayant eu plus de quatre à six partenaires sexuels auparavant 20,28,46,48,52,53,61. Cinq essais ont exclu les femmes ayant eu des frottis cervicaux anormaux 20,46,48,52,61 et trois autres ont exclu les femmes ayant eu des antécédents de colposcopie 26,28,44. L’essai CVT était le seul à ne pas comporter de restrictions fondées sur les verrues génitales ou les antécédents cervicaux ou sexuels 36. Ces restrictions peuvent faire en sorte que le vaccin semble plus efficace dans la population en intention de traiter (ITT) que dans la population générale de femmes du même âge. Dans l’étude CVT, l’efficacité dans le groupe ITT pour l’infection persistante à 12 mois par tout type de VPH oncogène était de 11 % (IC à 95 % : 2,2, 19,5) ; l’efficacité contre les CIN3+ n’a pas été démontrée dans le groupe ITT 36.
L’épidémiologie du VPH varie également d’un pays à l’autre, ce qui signifie que les résultats des essais peuvent être difficilement généralisables à certains contextes, y compris l’Afrique ; il est donc important de savoir si les résultats diffèrent selon la région étudiée. Aucun des essais portant sur les résultats d’efficacité n’a été mené en Afrique (nous n’avons connaissance que d’un essai d’innocuité et d’immunogénicité en Afrique 62), bien qu’il s’agisse de la région du monde où l’incidence du cancer du col de l’utérus est de loin la plus élevée 2. L’étude Cochrane reconnaît que « des différences dans la prévalence du HPV dans les sites d’essai, ou des différences dans les protocoles d’étude et les tests utilisés, peuvent expliquer le contraste d’efficacité » entre le Cervarix et le Gardasil 18
Quel est le risque de substitution oncogène du type de HPV ?
Les vaccins peuvent protéger contre des types de HPV qui ne sont pas inclus dans le vaccin. Il existe des preuves de protection croisée contre trois types de HPV à haut risque (31, 33 et 45) pour Cervarix (voir supplément 6) 31,36,43,45 . Il existe une protection croisée contre un type de HPV non inclus dans le vaccin par Gardasil 31 (voir supplément 6)63. Mais il existe des preuves d’un risque accru statistiquement significatif des types de HPV 51 et 58 dans les essais de Cervarix, par rapport au vaccin de contrôle 31,36. On ne sait pas si le ciblage du vaccin conduira à une substitution par d’autres types oncogènes, comme c’est le cas avec la vaccination antipneumococcique 64.
Facteurs méthodologiques des essais susceptibles d’affecter l’interprétation des résultats
Analyses multiples insuffisantes
Tous les essais ont procédé à de multiples analyses de sous-groupes, ce qui augmente la probabilité de résultats statistiques positifs en l’absence d’effet réel. Les définitions des sous-groupes varient d’un essai à l’autre, de sorte que les résultats ne peuvent être comparés d’un essai à l’autre. Les résultats n’ont pas été donnés pour tous les sous-groupes et n’ont pas été ventilés par pays, par site d’étude ou pour chaque résultat. Ce point est important étant donné les différences d’épidémiologie du HPV dans les différentes régions du monde. Il est possible que les données aient été rapportées de cette manière parce que l’incidence était faible. Nous avons inclus un tableau présentant les différentes définitions des sous-groupes dans le supplément 7.
Problèmes liés à la présentation des résultats des essais
Les essais rapportent l’efficacité du vaccin comme résultat primaire, ce qui montre la réduction relative du risque. Cela peut donner trop d’importance à l’efficacité par rapport à la réduction du risque absolu, comme le nombre de personnes à vacciner, qui est plus utile pour les cliniciens, les patients et les décideurs politiques. Aucun des essais n’a indiqué le nombre de vaccins nécessaires. L’essai CVT est le seul à avoir présenté des résultats en termes de réduction du risque absolu .36,38,39. La réduction du risque absolu de l’essai PATRICIA pour les CIN3+ dues à tout type de HPV oncogène (voir Supplément 4) (notre calcul) est de 0,75 %, ce qui donne un nombre nécessaire de 133 personnes à vacciner.
Fréquence du dépistage du cancer du col de l’utérus
Tous les essais ont effectué une cytologie de Pap à des intervalles de 6 à 12 mois. Le dépistage du cancer du col de l’utérus est recommandé en Angleterre tous les trois ans, entre 25 et 49 ans 65. L’augmentation de la fréquence du dépistage peut entraîner un surdiagnostic et un surtraitement des anomalies cytologiques qui devraient normalement se résorber et ne pas être détectées 66. L’augmentation de la fréquence des tests permet d’achever rapidement les essais, mais peut surestimer l’efficacité du vaccin.
Méthodes de dépistage du HPV
Les tests de positivité de l’ADN pour un type particulier de VPH (indiquant une infection en cours) et de séropositivité (indiquant une infection antérieure) ont une spécificité et une sensibilité limitées 67. C’est une autre raison pour laquelle l’infection par le VPH a des limites en tant que substitut du cancer du col de l’utérus. Seuls 50 à 70 % des infections à HPV donnent lieu à des réponses anti-HPV détectables 51, et la séropositivité initiale peut devenir négative 68. Des sous-groupes de femmes considérées comme naïves à l’égard du HPV peuvent donc avoir été exposées antérieurement. Par ailleurs, une infection latente peut être indétectable par les tests actuels. Le CIRC a noté qu' »on ne sait pas à quelle fréquence cette [infection latente] se produit chez les individus immunocompétents, combien de temps elle dure, ce qui provoque la réémergence dans un état détectable ou quelle fraction des cancers survient après une période de latence » 13 . Cela soulève également la question de savoir si les sous-groupes naïfs au VPH peuvent représenter de manière fiable les filles avant le début de leur vie sexuelle, et si l’infection par le VPH est un résultat de substitution valable.
Méta-analyse d’une valeur limitée en raison de l’hétérogénéité des essais
Les différences entre les critères d’évaluation des essais et les sous-groupes limitent la possibilité de comparer et d’agréger les données des essais. Cette situation est aggravée par le manque de normalisation entre les études pour toute une série de mesures : tests d’exposition antérieure au HPV, tests sérologiques pour détecter l’infection par le HPV et méthodes d’échantillonnage, y compris la fréquence des tests 67.
Il n’existe pas de critères convenus pour définir le type de VPH responsable des lésions cliniques, et les essais ont utilisé des critères différents (voir supplément 8). Il n’existe pas d’approche standard pour évaluer l’efficacité contre la maladie et l’infection dues à des types de HPV non présents dans le vaccin, par exemple pour savoir s’ils prenaient en compte les types oncogènes non vaccinaux ou tous les types de HPV non vaccinaux (voir le complément 9). Étant donné que Merck et GSK ont participé à tous les essais, on ne sait pas très bien pourquoi il n’y a pas eu de cohérence dans les méthodes et les tests d’un essai à l’autre.
Les recherches en cours sont-elles susceptibles de lever les incertitudes ?
Le présent document se concentre sur les essais contrôlés randomisés, mais nous avons également examiné si les études d’observation pouvaient répondre à certaines des incertitudes, en reconnaissant qu’il s’agit d’un niveau de preuve inférieur, mais pratiquement la source la plus probable d’informations futures en l’absence d’essais contrôlés randomisés à long terme. Nous avons identifié 19 études de suivi de phase 4, observationnelles et sans insu (y compris une méta-analyse d’études écologiques) qui sont potentiellement pertinentes pour les incertitudes discutées dans ce document (voir supplément 10). Aucune de ces études n’est idéale. Nombre d’entre elles sont de petite taille, de courte durée ou ne portent pas sur les CIN3+. Une étude d’observation (#5) a montré une réduction du risque relatif de CIN3 de 0,45 chez les personnes vaccinées 69 . Le suivi de l’essai PATRICIA (n° 3), le seul essai prévu 20 ans après la vaccination, et l’essai mexicain FASTER (n° 18) sont susceptibles de fournir davantage de données d’efficacité à long terme sur les critères d’efficacité les plus pertinents d’un point de vue clinique.
L’étude observationnelle récemment publiée, menée en Écosse par Palmer et al. 70 , apporte de nouvelles preuves de la réduction des CIN3+, quel que soit le type de HPV. Les auteurs notent les limites suivantes qui peuvent avoir gonflé les mesures d’efficacité : l’étude n’a recueilli des données que sur le premier cycle de dépistage du cancer du col de l’utérus à l’âge de 20 ans (maintenant modifié à l’âge de 25 ans en accord avec l’Angleterre) avec une sous-représentation du groupe non vacciné (23% de participation au dépistage contre 51% dans le groupe vacciné à l’âge de 20 ou 21 ans) ; et le temps de suivi plus court pour les femmes nées en 1995 et 1996 affecte nécessairement la robustesse de l’estimation de l’efficacité du vaccin pour les femmes plus jeunes. En outre, la base de l’affirmation de la protection de groupe n’est pas bien expliquée pour les femmes non vaccinées de la cohorte 1995-1996, par rapport aux femmes non vaccinées de 1988-1990. Les auteurs n’examinent pas non plus comment les changements dans l’activité sexuelle ont pu contribuer à la diminution observée de la prévalence de la CIN indépendamment du vaccin : entre 2002 et 2014 (la dernière période pour laquelle il existe des données), la proportion de jeunes écossais de 15 ans ayant déjà eu des rapports sexuels a diminué, bien que des inégalités socio-économiques persistent en ce qui concerne l’initiation sexuelle et l’utilisation de préservatifs 71. Le recours au dépistage varie également en fonction du statut socio-économique 72.
Que devons-nous faire face à l’incertitude ?
Sur le plan politique
Nous demandons aux décideurs politiques de :
1. Établir des données épidémiologiques nationales de référence sur l’incidence du cancer, la mortalité et la prévalence des sous-types de HPV afin de soutenir les décisions fondées sur des données probantes quant à la question de savoir si les vaccins actuellement disponibles sont susceptibles d’être rentables et s’ils devraient constituer une priorité.
2. Veiller à ce que la surveillance du cancer et les registres soient en place avant la mise en œuvre de tout programme de vaccination, afin de pouvoir étudier l’évolution de l’incidence du cancer du col de l’utérus et de ses précurseurs.
3. Lancer des études nationales à long terme sur l’efficacité et l’efficience qui ne soient pas financées par l’industrie, qui se concentrent sur des résultats cliniquement significatifs, et qui recrutent et analysent les populations cibles des vaccins.
La recherche
Au Royaume-Uni, on estime que le dépistage du cancer du col de l’utérus prévient plus de 80 % des cancers du col de l’utérus 15. Une analyse coût-efficacité réalisée en Australie suggère que la vaccination n’est pas rentable dans les contextes où le dépistage du cancer du col de l’utérus est établi 73 . Nous ne savons toujours pas combien de cas de maladies du col de l’utérus évités par la vaccination auraient été détectés par le dépistage du cancer du col de l’utérus. Nous ne savons toujours pas combien de cas de maladie cervicale évités par la vaccination auraient été détectés par le dépistage du col de l’utérus. L’encadré 2 (Box 2) présente nos recommandations pour la poursuite de la recherche afin de lever les incertitudes. Nous demandons également que la recherche sur le papillomavirus ne soit pas financée par l’industrie.
Encadré 2. Recommandations pour de futurs essais afin de lever les incertitudes.
– Vacciner avant le début de l’activité sexuelle et commencer l’évaluation des critères d’évaluation à l’âge du dépistage cervical habituel une fois que l’on est sexuellement actif.
– Rendre publics tous les rapports d’études cliniques, y compris les données individuelles anonymes des patientes.
– Séparer les essais pour évaluer les bénéfices chez les femmes déjà exposées au HPV, sans restrictions basées sur les facteurs de risque.
– Analyser les données par pays et par site d’étude.
– Veiller à ce que l’intervalle entre les tests soit conforme aux protocoles habituels de dépistage du cancer du col de l’utérus.
– Poursuivre le suivi pendant au moins 20 ans à partir de l’entrée dans la vie sexuelle.
– Établir la puissance des essais pour le résultat composite principal CIN3/AIS/cancer du col de l’utérus dû à des types de HPV oncogènes.
– Définir le résultat secondaire de l’infection persistante par le HPV 16/18 après au moins 12 mois.
– Utiliser des méthodes de test standardisées pour la détection du HPV.
– Entreprendre un essai d’efficacité du Gardasil-9 contrôlé par placebo avec une solution saline chez des participantes non vaccinées auparavant, car il est difficile de tirer des conclusions sur l’efficacité et le risque d’effets nocifs sur la base de l’essai comparant le Gardasil-9 au Gardasil.
Conclusion
Cet examen a révélé de nombreux problèmes méthodologiques dans les essais d’efficacité de phase 2 et 3 de la vaccination anti-HPV, ce qui entraîne des incertitudes quant à la compréhension de son efficacité.
1. Cancer du col de l’utérus – Il n’est pas certain que la vaccination contre le HPV prévienne le cancer du col de l’utérus. Les essais n’ont pas été conçus pour détecter ce résultat, qui prend des décennies à se développer. Pour la plupart des résultats, les données de suivi n’existent en moyenne que pour quatre ou cinq ans.
2. CIN – Il existe des preuves que la vaccination prévient la CIN1 ; toutefois, il ne s’agit pas d’un résultat cliniquement important (aucun traitement n’est administré). Les essais ont utilisé des résultats de substitution composites incluant la CIN1, mais une efficacité élevée contre la CIN1+ (CIN1, 2, 3 et AIS) ne signifie pas nécessairement une efficacité élevée contre la CIN3+ (CIN3 et AIS), qui survient beaucoup moins fréquemment. Les données sont trop peu nombreuses pour que l’on puisse conclure clairement que le vaccin anti-HPV prévient les CIN3+. Il est probable que les CIN en général aient été surdiagnostiquées dans les essais, car la plupart d’entre eux ont effectué une cytologie cervicale à des intervalles de 6 à 12 mois plutôt qu’à l’intervalle normal de dépistage de 36 mois. Cela signifie que les essais ont peut-être surestimé l’efficacité du vaccin, car certaines lésions auraient régressé spontanément.
3. Infection persistante par le HPV – Les résultats de l’infection par le HPV sont difficiles à interpréter. De nombreux essais ont diagnostiqué une infection persistante sur la base de tests fréquents à intervalles courts, c’est-à-dire moins de six mois. Cela ne permet pas de savoir si les infections détectées disparaissent ou persistent et entraînent des modifications du col de l’utérus. Dans le programme actuel de dépistage du cancer du col de l’utérus de Public Health England, les patientes qui sont positives au HPV mais dont la cytologie est négative ne sont pas testées à nouveau avant 12 mois 74.
4. Différences entre les essais et les populations réelles – La plupart des participants aux essais étaient plus âgés que les enfants de 9 à 13 ans à qui l’on propose généralement la vaccination. L’efficacité chez les filles âgées de 9 à 13 ans a été estimée à l’aide d’essais de pontage immunitaire (où les niveaux de réponse immunitaire sont mesurés) plutôt qu’à l’aide de résultats d’efficacité clinique 60. Nous ne savons pas quel niveau de titres d’anticorps protège contre le cancer du col de l’utérus et ses précurseurs, ni combien de temps la protection durera60 . De même, les données sur les résultats obtenus chez les femmes de plus de 24 ans sont limitées et tous les essais, à l’exception du Costa Rica Vaccine Trial (CVT), comportaient des exclusions liées aux antécédents sexuels ou aux antécédents de verrues génitales ou de maladies du col de l’utérus, ce qui limite la généralisation aux populations vaccinées en rattrapage 36. L’épidémiologie du VPH varie d’un pays à l’autre. Aucune étude d’efficacité n’a été réalisée en Afrique.
5. Protection croisée et substitution de types de HPV – Il n’est pas certain que le vaccin assure une protection croisée contre les types de HPV oncogènes non ciblés par les vaccins. Il existe également un risque de substitution, lorsqu’un type de HPV oncogène non ciblé par le vaccin comble le vide laissé par la réduction d’un type de HPV ciblé par les vaccins.
6. Considérations méthodologiques – De nombreux essais comportaient de multiples analyses de sous-groupes manquant de puissance, ce qui augmente le risque de résultats faussement positifs. Tous les essais, à l’exception du CVT, ont rapporté des effets relatifs plutôt qu’absolus, ce qui tend à surestimer l’efficacité, et aucun n’a fourni le nombre de personnes à vacciner.
Remerciements
Nous remercions Peter Roderick pour ses commentaires sur les versions préliminaires et son aide à la rédaction, ainsi que les réviseurs et l’équipe éditoriale du BMJ (NdT : British Medical Journal, une des revues les plus prestigieuses au Monde dans le domaine médical). Nous souhaitons également remercier l’équipe PPI de l’université de Newcastle pour ses commentaires utiles.
Conflits d’intérêt
Aucun conflit d’intérêt déclaré
Financement
Aucun financement déclaré
Déclarations
Approbation éthique
Sans objet.
Garant
AMP.
Contribution
L’AMP a eu l’idée de l’article ; le CPR a effectué l’analyse de la littérature et rédigé les premières versions de l’article ; le CPR, l’AMP et PB ont contribué à l’analyse et à la reformulation de l’article.
Provenance
Pas de commande ; révision éditoriale des commentaires d’une autre revue et révision ultérieure.
Matériel supplémentaire
Le matériel supplémentaire pour cet article est disponible en ligne.
Références
Les références sont dans l’article original :
https://journals.sagepub.com/doi/10.1177/0141076819899308
S’il vous plaît, diffusez largement la dénonciation de la fraude du vaccin HPV !
Si Dieu le veut, nous contribuerons, avec un peu de chance, à sauver quelques enfants de cette tragédie.
Traduction Jean Bitterlin 24 mars 2023
Par Jamila Buret
⚠ Les points de vue exprimés dans l’article ne sont pas nécessairement partagés par les (autres) auteurs et contributeurs du site Nouveau Monde.